4月6日,安进宣布其重磅药物TEPEZZA®(teprotumumab-trbw)通过贴敷式注射器进行皮下注射,治疗中度至重度活动性甲状腺眼病(TED)成人患者的3期临床试验获得了积极的顶线结果,为患者带来更加便捷、且疗效媲美静脉输注(IV)的全新给药选择!
TEPEZZA静脉注射(IV)剂型曾于2020年获批,是目前全球首个也是唯一一个获批用于治疗甲状腺眼病的药物。通过靶向疾病的根本原因,TEPEZZA彻底改变了TED的治疗格局,至今已在全球惠及超过25,000名患者。
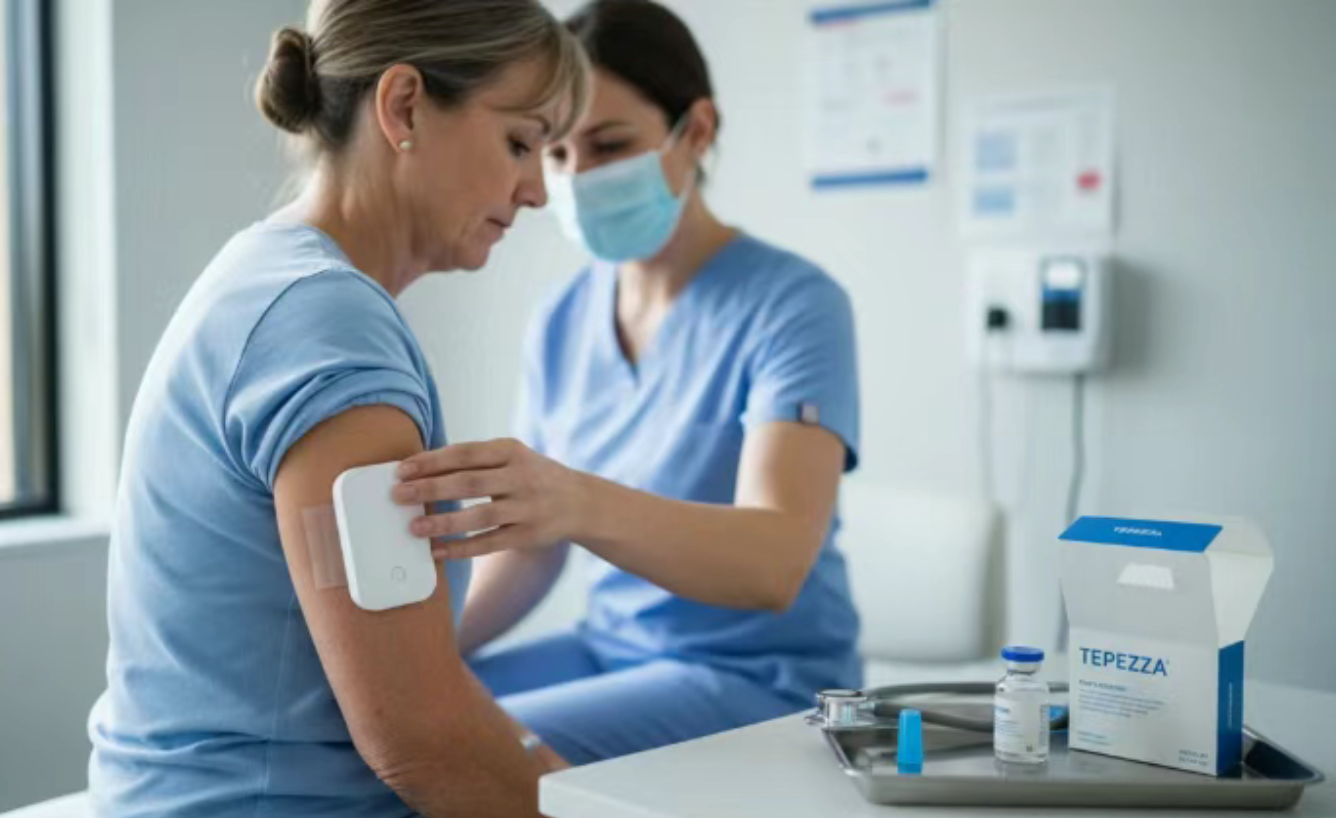
临床数据:77%患者实现突眼显著缓解
本次公布的3期临床试验数据令人振奋,研究成功达到了主要终点。在为期24周的安慰剂对照期内,接受TEPEZZA皮下注射治疗的患者展现出了具有高度统计学意义和临床意义的突眼缓解率。
-
主要终点: 高达76.7%的TEPEZZA皮下注射组患者实现了突眼缓解,而安慰剂组仅为19.6%(p<0.0001)。
-
关键次要终点: 在第24周时,治疗组患者的平均突眼减少量达到了 -3.17毫米,相比之下,安慰剂组仅为-0.80毫米(p<0.0001)。超过3毫米的突眼减少对于患者而言具有极其重要的临床意义,能够显著改善患者的眼部外观和舒适度。
此外,该试验还在多个关键次要终点上取得了具有统计学意义和临床意义的改善,包括:总体应答率、达到临床活动评分(CAS)0或1的患者比例、复视(双影)的改善程度、复视应答率、完全复视应答率,以及在第24周Graves眼病生活质量(GO-QoL)外观子量表的平均基线变化。
在安全性方面,TEPEZZA皮下注射的总体安全性结果与TEPEZZA静脉注射剂型(IV)的已知安全性特征基本一致。部分患者在使用皮下给药时观察到了轻度至中度的注射部位反应,但这些反应并未导致治疗的中断或停药。最常见的不良事件(发生率≥10%)包括:肌肉痉挛、耳鸣、体重下降、耳部不适、恶心和腹泻。值得注意的是,参与该研究的患者中包含了基线时存在听力损伤的患者,这也是该试验设计的一大特点。
临床试验设计
本次3期临床试验是一项随机、双盲、安慰剂对照、平行组、多中心的研究。参与者在研究期间每两周通过贴敷式注射器(OBI)接受一次TEPEZZA或安慰剂的皮下注射,共计12次注射。入组标准要求患者在15个月内确诊为中度至重度活动性TED,且基线突眼度≥3毫米。
此外,安进还同时宣布完成了一项针对TEPEZZA静脉剂型的独立3b/4期试验(为满足FDA的上市后要求)。该研究评估了三种不同治疗持续时间(4次、8次和16次输注)的安全性、耐受性以及再次治疗的需求,其观察到的风险特征同样与TEPEZZA的已知情况一致。
关于甲状腺眼病(TED)
甲状腺眼病(TED)是一种严重的、进行性的、且可能威胁视力的罕见自身免疫性疾病。它通常发生于Graves病患者中,但本质上是一种独立的疾病。由于自身抗体激活了眼眶后空间细胞上的胰岛素样生长因子-1受体(IGF-1R)介导的信号复合体,引发了一系列可能威胁视力的炎症和组织生长反应。TED的早期症状包括眼睛干涩、红肿、流泪过多、眼睑退缩、眼球突出(突眼)、眼球后部压力或疼痛以及复视(双影)。在中国约有400万患者。