2026年5月12日,德国家族制药巨头勃林格殷格翰(Boehringer Ingelheim, BI)宣布与临床阶段生物技术公司 Immunitas Therapeutics 达成一项总额高达4.075亿欧元(约4.78亿美元)的全球独家授权协议。
此次交易的核心是一款处于临床前阶段、针对慢性炎症与自身免疫性疾病(AID)的候选抗体。尽管具体靶点在新闻稿中受商业保护而未完全公开,但结合Immunitas的研发底色与近期学术产出,业界普遍认为该项目直指CD161(KLRB1)这一极具潜力的免疫调节靶点。
核心逻辑:从“细胞因子阻断”向“致病细胞耗竭”的范式转移
在过去的二十年中,自免领域的研发重心集中在下游细胞因子的拦截(如 TNF-α、IL-17、IL-23 等)。然而,随着部分患者产生耐药以及对“深度缓解”需求的提升,研发策略正经历从免疫抑制(Immune Suppression)向免疫重塑(Immune Resetting)的演进。
Immunitas 提出的策略并非单纯阻断信号,而是选择性清除致病性 T 细胞。其背后的生物学底层逻辑如下:
-
CD161 靶点的特异性:CD161(由 KLRB1 基因编码)高表达于多种促炎性免疫细胞表面,特别是Th17 细胞和部分产生 IL-17 的CD8+T 细胞(Tc17)。这些细胞是克罗恩病(CD)、银屑病及类风湿性关节炎等多种自免疾病的关键驱动者。
-
Fc 工程化的精准打击: 与其在肿瘤领域采用Fc减弱(Fc-attenuated)以恢复 T 细胞活性的IMT-009不同,自免项目(推测为IMT-380 系列)采用了Fc 增强(Fc-active)策略。通过ADCC/ADCP效应,抗体能够精准耗竭表达 CD161 的致病细胞,从而从上游“切除”炎症源头,理论上可提供比细胞因子抑制剂更持久的临床获益。
技术底色:单细胞基因组学驱动的靶点挖掘
Immunitas 的核心竞争力在于其由 Aviv Regev 等顶尖科学家创立的单细胞基因组学发现引擎。
在自免疾病的异质性面前,传统的体外模型往往难以模拟复杂的免疫微环境。Immunitas 利用单细胞测序技术,在人源样本中识别出特定疾病状态下起核心作用的“节点细胞”。此次 BI 愿意为临床前资产支付超 4 亿欧元溢价,很大程度上是对该平台靶点验证(Target Validation)深度的认可。
BI 的自免版图:构建“多机制驱动”的防御护城河
进入 2026 年,勃林格殷格翰在自免领域的布局密度显著增加,呈现出明显的矩阵化特征:
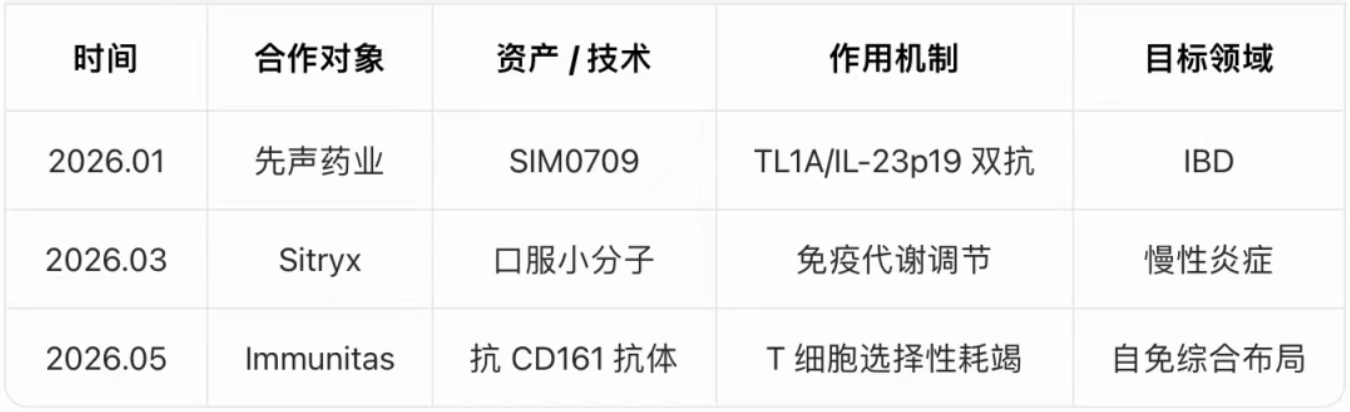
BI 的策略正从单一路径转向“全栈式”布局。通过 SIM0709 覆盖经典的细胞因子通路,通过 Sitryx 探索代谢重编程,而此次通过 Immunitas 介入细胞清除疗法,BI 正在补齐其在“免疫重塑”领域的最后一块拼图。相比目前火热但受限于适应症的 B 细胞清除方案(如 CD19/CD20 靶点),靶向 T 细胞的方案在纤维化和某些特定炎症疾病中具有更广阔的差异化空间。
风险与挑战:前路非坦途
尽管科学故事引人入胜,但在药物研发专业人士眼中,该项目仍需面对重重挑战:
1.安全窗口(Safety Window): 大规模耗竭 T 细胞亚群是否会带来严重的免疫缺陷或机会性感染风险?
2.Abcuro 的前车之鉴: 此前靶向 KLRG1 旨在清除致病 T 细胞的药物 ulviprubart 在后期临床中遭遇挫折,提醒业界“选择性清除”在人体内的实际表现(如代偿性免疫通路的激活)远比模型复杂。
3.生物标志物(Biomarkers): 如何精确定义并筛选出最能从“CD161+ 细胞耗竭”中获益的患者群体,将是 Phase 1b/2 阶段 PoC(概念验证)成败的关键。
总结
勃林格殷格翰与 Immunitas 的合作,标志着 MNC(跨国药企)对自免疗法的底层逻辑正在发生深刻变革。从“阻断信号”到“清除细胞”,这不仅是技术手段的升级,更是对自免疾病治愈可能性的又一次冲击。
对于研发专业人士而言,CD161 靶点的人体数据将成为下一个十年自免领域最值得关注的变量之一。