一、 研究背景
尿路上皮癌(UC)是一种常见的癌症,全球每年有61.4万新发病例和22万膀胱癌死亡病例。
9MW2821(Bulumtatug Fuvedotin, BFv)是一种搭载MMAE毒性载荷的新一代靶向Nectin-4的抗体偶联药物(ADC)。
特瑞普利单抗(Toripalimab)是一种新型重组人源化抗PD-1单克隆抗体,已在中国、美国等国家获批。
既往研究表明,BFv在含铂化疗和免疫检查点抑制剂治疗后进展的局部晚期或转移性尿路上皮癌(la/mUC)患者中显示出可喜的疗效。
二、 研究设计与基线特征

研究设计:这是一项在中国开展的1b/II期、开放标签、多中心研究,包含剂量递增和队列扩展阶段。
给药方案:每21天为一个周期,患者在第1天和第8天接受BFv(1.0或1.25mg/kg),在第1天接受特瑞普利单抗(240mg)。
研究终点:主要终点为安全性;次要终点包括疗效、药代动力学(PK)和免疫原性。
患者基线:截至2025年4月30日,共有40名未经治疗(初治)的la/mUC患者被纳入初步疗效数据分析。这些患者的中位年龄为67岁,其中70.0%为男性,82.5%的患者Nectin-4表达为阳性。
三、 疗效与安全性数据
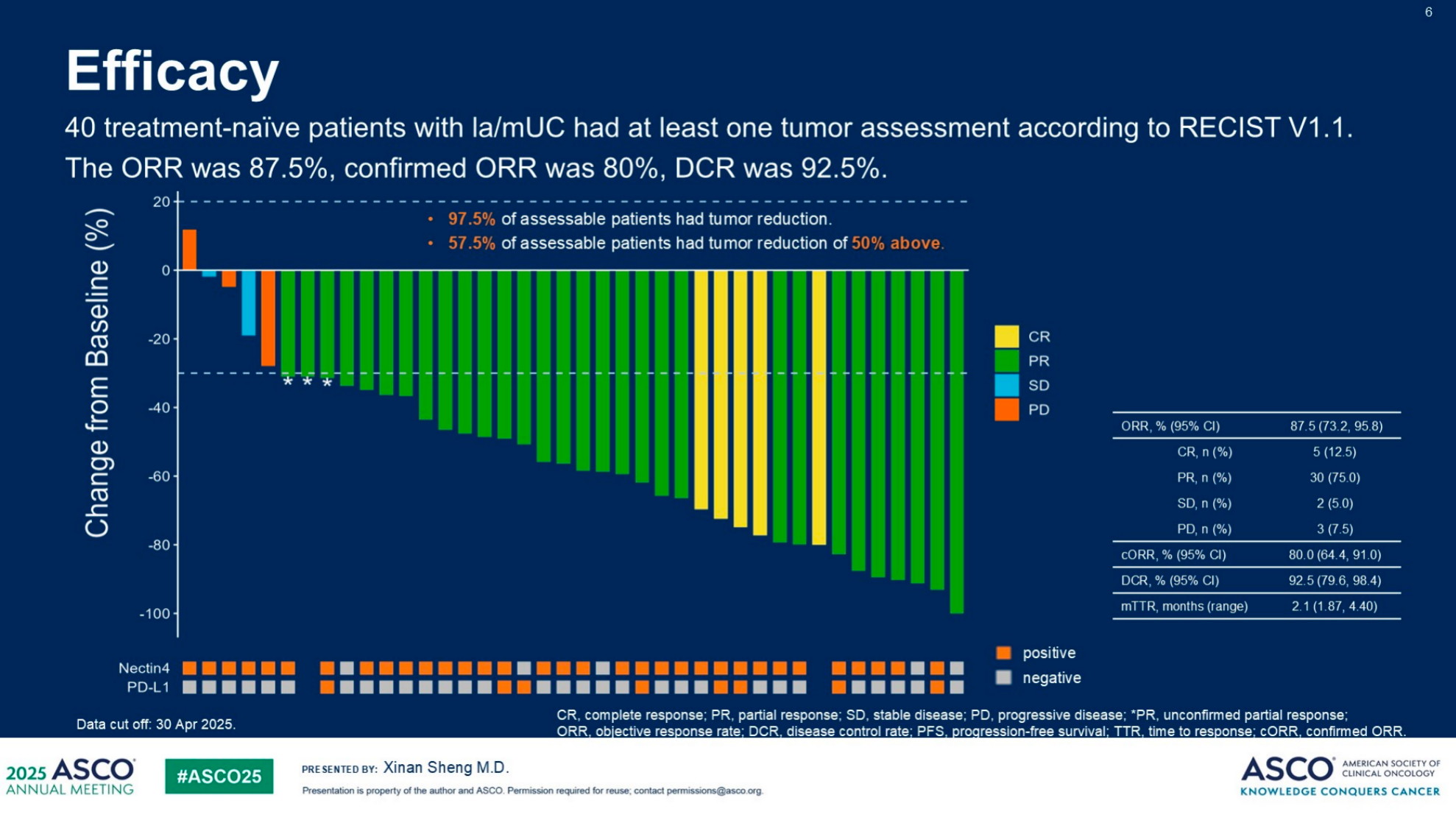
核心疗效指标:在40名初治la/mUC患者中,客观缓解率(ORR)达到87.5%,确认的客观缓解率(cORR)为80.0%,疾病控制率(DCR)高达92.5%。
肿瘤缩小情况:97.5%的可评估患者出现了肿瘤缩小,其中57.5%的患者肿瘤缩小程度达到50%以上。完全缓解(CR)率为12.5%,部分缓解(PR)率为75.0%。
亚组分析:无论原发肿瘤部位、是否存在肝转移,以及Nectin-4和PD-L1的表达情况如何,不同亚组的初治患者均能从该联合疗法中获益,且获益情况与总体人群一致。
生存期数据:在中位随访时间10.8个月时,中位无进展生存期(mPFS)尚未成熟,初步数据为12.5个月(95% CI: 6.47-NA)。
安全性:安全性特征与既往BFv和特瑞普利单抗的试验结果一致,研究中未观察到新的安全性信号。
四、 核心结论
9MW2821联合特瑞普利单抗在初治局部晚期或转移性尿路上皮癌患者中展现出了令人鼓舞的疗效和可控的安全性,该联合疗法有望为尿路上皮癌患者提供一种全新的治疗选择。