3月28日,Biogen 在2026年美国皮肤病学会(AAD)年会上重磅宣布:其在研创新疗法 Litifilimab(BIIB059)在治疗皮肤红斑狼疮(CLE)的 AMETHYST II/III期临床研究的II期部分(A部分)中,成功达到主要终点,显著降低了患者的皮肤疾病活动度!
这是 Litifilimab 取得的第二个阳性II期临床结果。作为目前唯一在多项CLE研究中展现出持续、积极疗效的在研项目,Litifilimab有望成为该疾病70年来的首款靶向疗法。
关于 Litifilimab
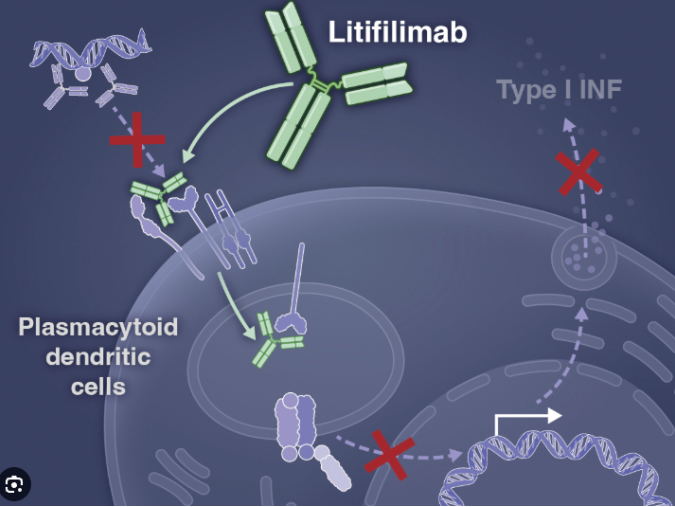
Litifilimab 由 Biogen 自主研发,是首个靶向血液树突状细胞抗原2(BDCA2)的人源化IgG1单克隆抗体。BDCA2主要表达于人体的浆细胞样树突状细胞(pDCs)表面。研究表明,Litifilimab与BDCA2结合后,能够有效抑制pDCs产生包括I型干扰素(IFN-I)在内的促炎分子,而这些炎症介质正是导致系统性和皮肤红斑狼疮发病的关键元凶。
凭借其出色的早期数据,Litifilimab此前已获得美国FDA授予的突破性疗法认定(Breakthrough Therapy Designation)。
临床数据:起效迅速,显著改善皮损
本次公布的AMETHYST是一项正在进行的无缝两阶段、多中心、双盲、安慰剂对照的随机试验。其A部分(第0-24周)的数据令人兴奋:
-
达到主要终点:在第16周时,通过皮肤红斑狼疮活动度研究者总体评估修订版(CLA-IGA-R)红斑评分(0-1分,即皮损完全清除或几乎清除)来衡量,Litifilimab组患者的疾病活动度降低比例达到了14.7%,而安慰剂组仅为2.9%(差异达11.8%,p < 0.05)。
-
起效迅速且疗效持久:Litifilimab在第4周就观察到了与安慰剂的疗效分离。到第24周时,40.8%的Litifilimab组患者达到了CLASI-50响应(即CLASI-A评分较基线改善50%),而安慰剂组为21%。
-
更高比例实现深度缓解:在第24周,Litifilimab组有21.7%的患者达到CLASI-70响应(安慰剂组为5.8%);更有**六分之一(16.3%)**的Litifilimab组患者实现了CLASI 0-3评分(即无或极轻微的疾病活动),而安慰剂组这一比例为0%。
-
安全可靠,耐受性表现良好:在AMETHYST研究的A部分中,Litifilimab表现出了良好的耐受性。在24周内,Litifilimab组和安慰剂组出现不良事件(AE)的比例分别为74.6%和64.7%,且绝大多数不良事件为轻度至中度。严重不良事件的发生率在两组中分别为6.8%和2.9%。
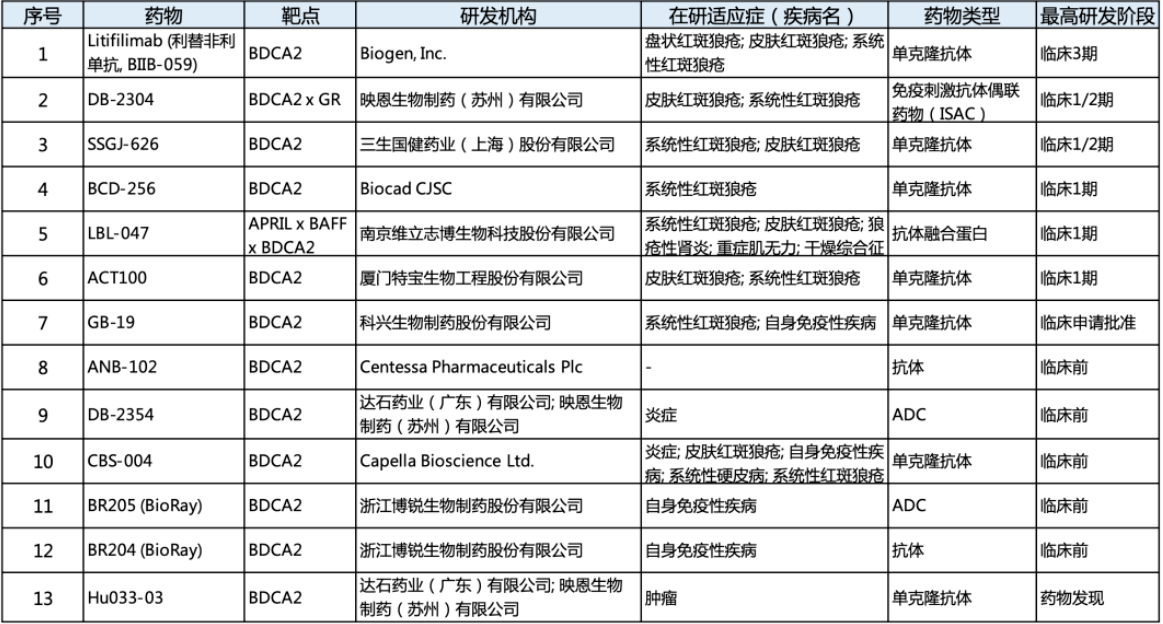
BDCA2全球在研管线