Poster 链接:https://pharmato.cn/poster-share/WTNC2LOYrBYn5FQMlqwo5wh1l09SBQDn
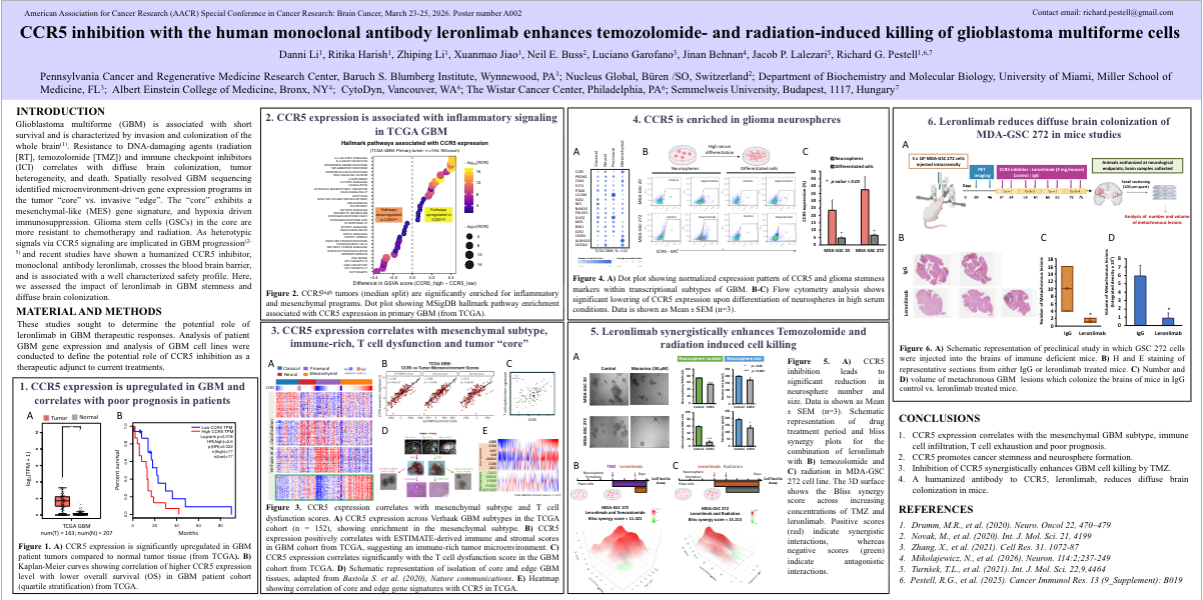
1. 核心洞察:CCR5 是 GBM 的“致命弱点”
胶质母细胞瘤(GBM)因其高度侵袭性和对标准疗法的抗性而难以攻克 。研究发现,CCR5 受体在 GBM 中显著上调,且与患者的生存预后呈负相关 。
-
预后风险:高 CCR5 表达患者的中位生存期仅约 13-15 个月,而低表达组约为 22-25 个月 。
-
致死率增加:高表达组的死亡风险是低表达组的 2.6 倍 ( p=0.022 ) 。
-
亚型富集:CCR5 专门富集在最具侵袭性、最易耐药的间质型 (Mesenchymal) GBM 中 。
2. 机制揭秘:为什么针对 CCR5 有效?
CCR5 不仅仅是一个标记物,它深度参与了肿瘤的“干性”维持和微环境塑造 。
-
维持肿瘤干细胞:CCR5 在胶质瘤神经球(GSCs)中高度表达 。
-
塑造抑制性微环境:CCR5 表达与 T 细胞功能障碍(衰竭) 信号强正相关 。
-
驱动炎症信号:它与 IL6/JAK/STAT3 和 TNFA 等促癌炎症通路密切相关 。
3. 治疗突破:Leronlimab 的双重打击
Leronlimab 是一种人类单克隆抗体,研究证实它能有效阻断 CCR5 信号通路 。
A. 协同增敏:让放化疗“威力倍增”
实验显示,Leronlimab 能够显著增强标准疗法的杀伤力(Bliss 协同得分 > 10 即为强协同):
-
联合替莫唑胺 (TMZ):协同得分高达 11.421 。
-
联合放射治疗 (Radiation):协同得分高达 15.215 。
B. 阻断扩散:遏制脑部定植
在动物实验中,Leronlimab 展示了极其出色的抗转移能力 :
-
病灶数量锐减:对照组小鼠脑内平均产生 10 个继发病灶,而治疗组仅为 1-2 个 。
-
肿瘤体积萎缩:继发病灶的总负担(集成密度)从 6.0 \times 10^7 降低至 1.0 \times 10^7 。
4. 结论与临床前景
-
精准打击:Leronlimab 能够跨越血脑屏障,直接靶向耐药的肿瘤干细胞 。
-
安全性高:该抗体具有良好的安全记录,支持其作为辅助疗法进入临床 。
-
逆转耐药:通过抑制 CCR5,可以有效“翻转”间质型 GBM 的侵袭特性,提高患者生存希望 。