引言
针对不可切除或转移性尿路上皮癌(mUC)患者的一线治疗,医学界一直在探索更有效、更持久的治疗方案。在2025年的美国临床肿瘤学会(ASCO)年会上,研究人员公布了备受瞩目的CheckMate 901试验(NCT03036098)的最终结果。本次报告特别聚焦于那些不适合接受顺铂化疗(cisplatin-ineligible)的患者群体,评估了“双免疗法”——纳武利尤单抗(Nivolumab,O药)联合伊匹木单抗(Ipilimumab,Y药)相较于标准吉西他滨联合卡铂(Gem-Carbo)化疗的临床表现。
研究设计与患者基线
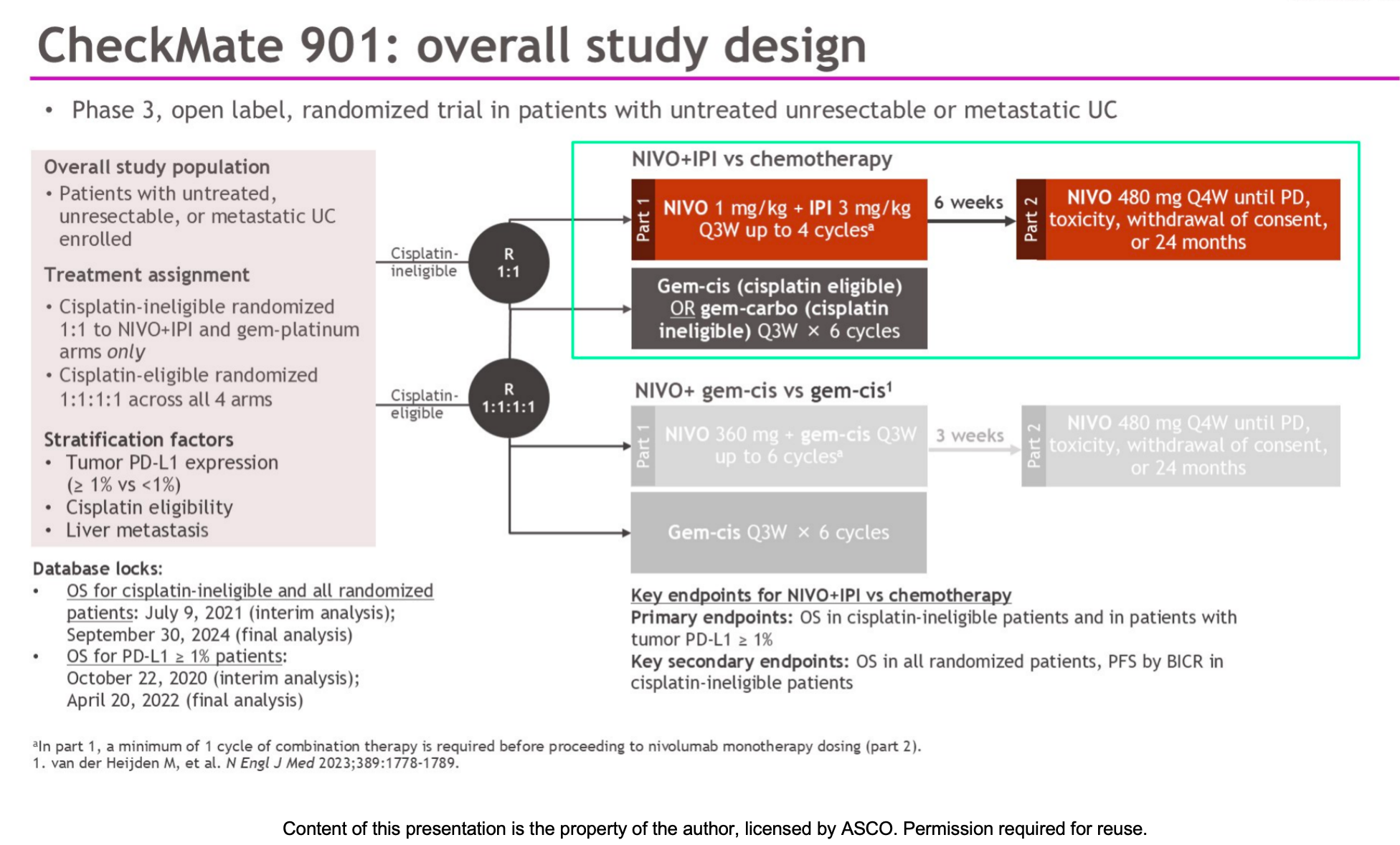
CheckMate 901是一项全球性、开放标签的3期随机临床试验。在这一特定队列中,共有445名既往未接受过治疗且不适合顺铂(肾小球滤过率在30至<60 mL/min之间)的转移性或不可切除尿路上皮癌患者参与。 患者被按1:1的比例随机分配至两组:
-
免疫联合组(221人):接受纳武利尤单抗(1 mg/kg)+ 伊匹木单抗(3 mg/kg),每3周一次,最多4个周期;随后接受纳武利尤单抗单药维持治疗,直到疾病进展或出现不可耐受的毒性(最长两年)。
-
化疗组(224人):接受标准的吉西他滨联合卡铂化疗。 研究的主要终点为总生存期(OS),次要和探索性终点包括无进展生存期(PFS)、客观缓解率(ORR)、缓解持续时间(DOR)以及安全性。
核心疗效数据:
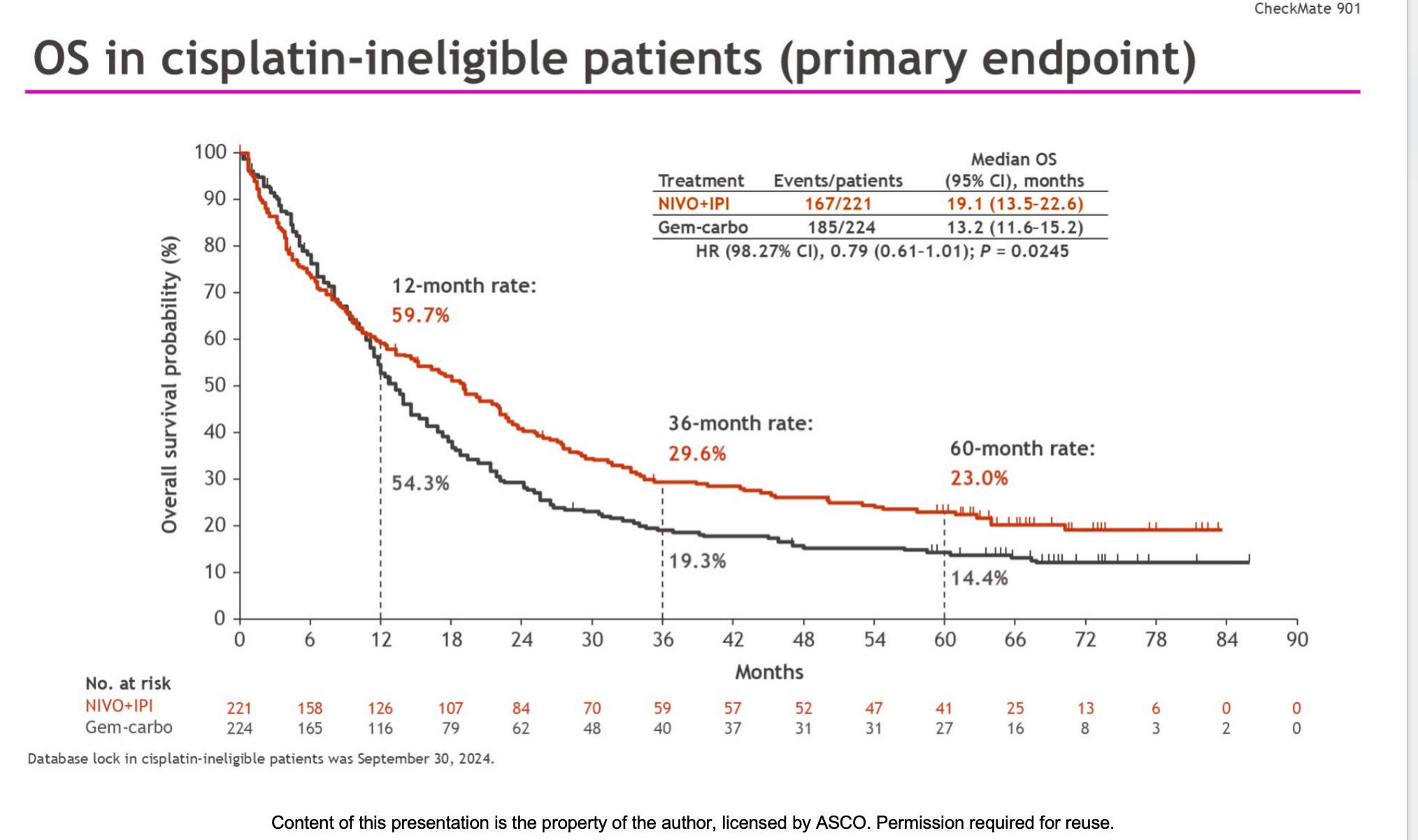
未达统计学显著性,但长期获益明显 经过中位58.3个月的长期随访,研究结果揭示了两种疗法的不同特点:
-
总生存期(OS):免疫联合组的中位OS为19.1个月,而化疗组为13.2个月(风险比 HR=0.79 [98.27% CI, 0.61–1.01];P = 0.0245)。遗憾的是,根据试验预设的严格统计学门槛,这一总生存期的改善未能达到统计学显著性。
-
客观缓解与缓解持续时间(DOR):两组的客观缓解率(ORR)相近(免疫组35.3% vs 化疗组38.8%)。然而,免疫疗法在起效后的持久性上展现了巨大的优势。免疫联合组的中位缓解持续时间(mDOR)高达25.0个月,是化疗组(7.4个月)的三倍以上。
-
长期生存率(Landmark OS):在随访至36个月时,免疫联合组的OS率达到29.6%,明显高于化疗组的19.3%。
安全性与耐受性
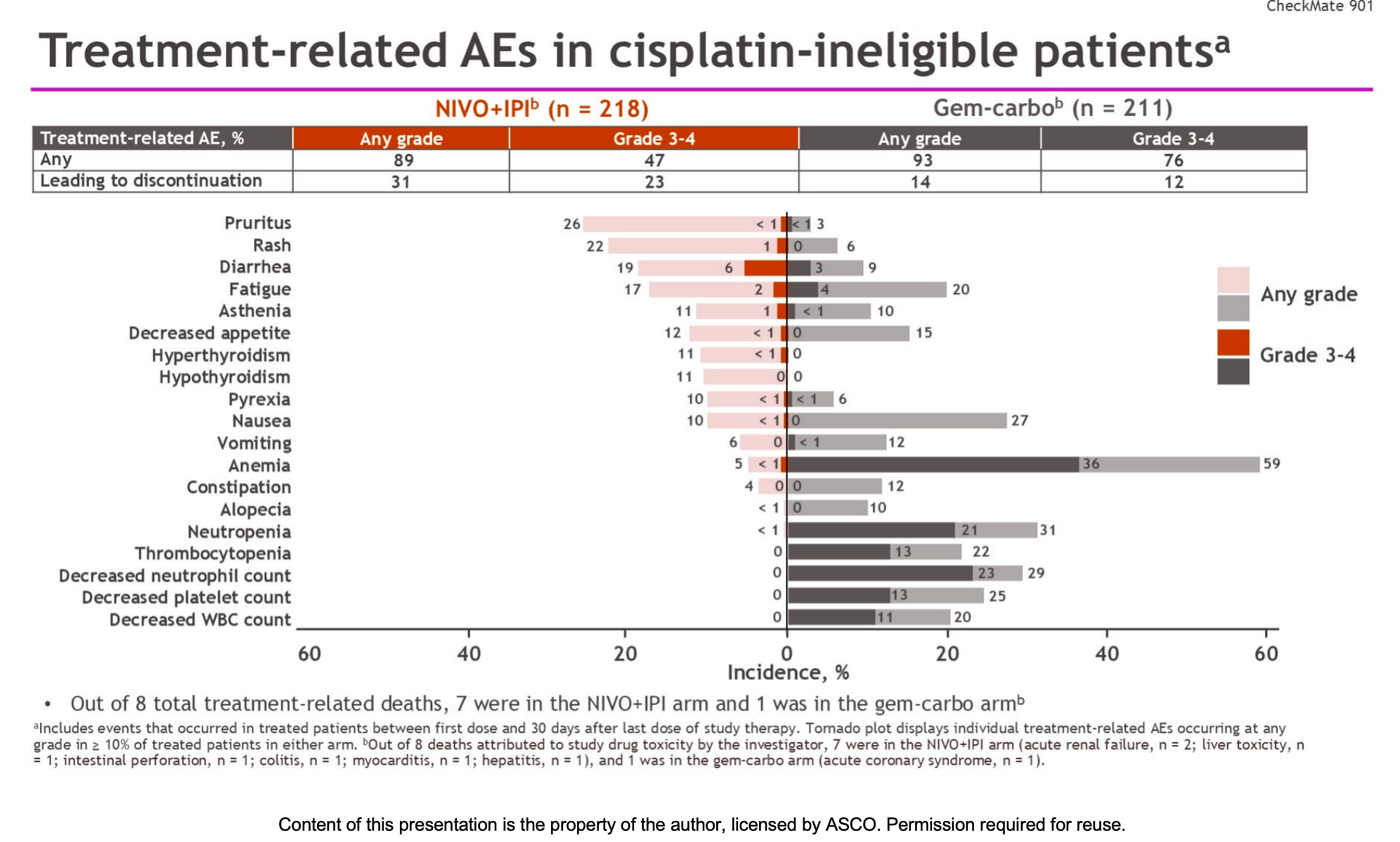
在安全性方面,未发现新的安全信号。
-
免疫联合组任意级别的治疗相关不良事件(TRAEs)发生率为89.0%,其中3-4级重度不良事件占比为47.2%。
-
化疗组任意级别TRAEs发生率为92.9%,但其3-4级不良事件发生率明显更高,达到了76.3%(主要由于化疗带来的血液学毒性)。
-
然而,免疫联合组因不良事件导致治疗中断的比例较高(31.2% vs 化疗组的14.2%),主要与免疫相关不良反应有关。
结论与临床意义
综上所述,在不适合接受顺铂化疗的晚期尿路上皮癌一线治疗中,纳武利尤单抗联合伊匹木单抗虽然在总生存期(OS)上未能跨过统计学显著性的阈值,但其带来了极具临床意义的持久缓解(DOR长达25个月)和良好的长期生存率。
这一结果表明,对于部分患者而言,这种有限疗程的“去化疗(chemotherapy-free)”双重免疫方案依然具有实质性的临床抗肿瘤活性。未来的研究方向可能需要聚焦于生物标志物的探索,以便在临床实践中更精准地筛选出能从该双免疗法中获得长期生存的优势获益人群。