5月7日,美国生物技术公司Entrada Therapeutics宣布了其治疗杜氏肌营养不良症(DMD)的在研新药ENTR-601-44的一项早期临床积极顶线数据。
数据显示,Entrada 的 ENTR-601-44(外显子 44 跳过疗法)Phase 1/2 试验:肌营养不良蛋白水平仅提升 2.36%,远低于公司原先设定的10%以上的提升预期,Entrada的股价在当天盘前直接暴跌57%。
关于ENTR-601-44和EEV平台
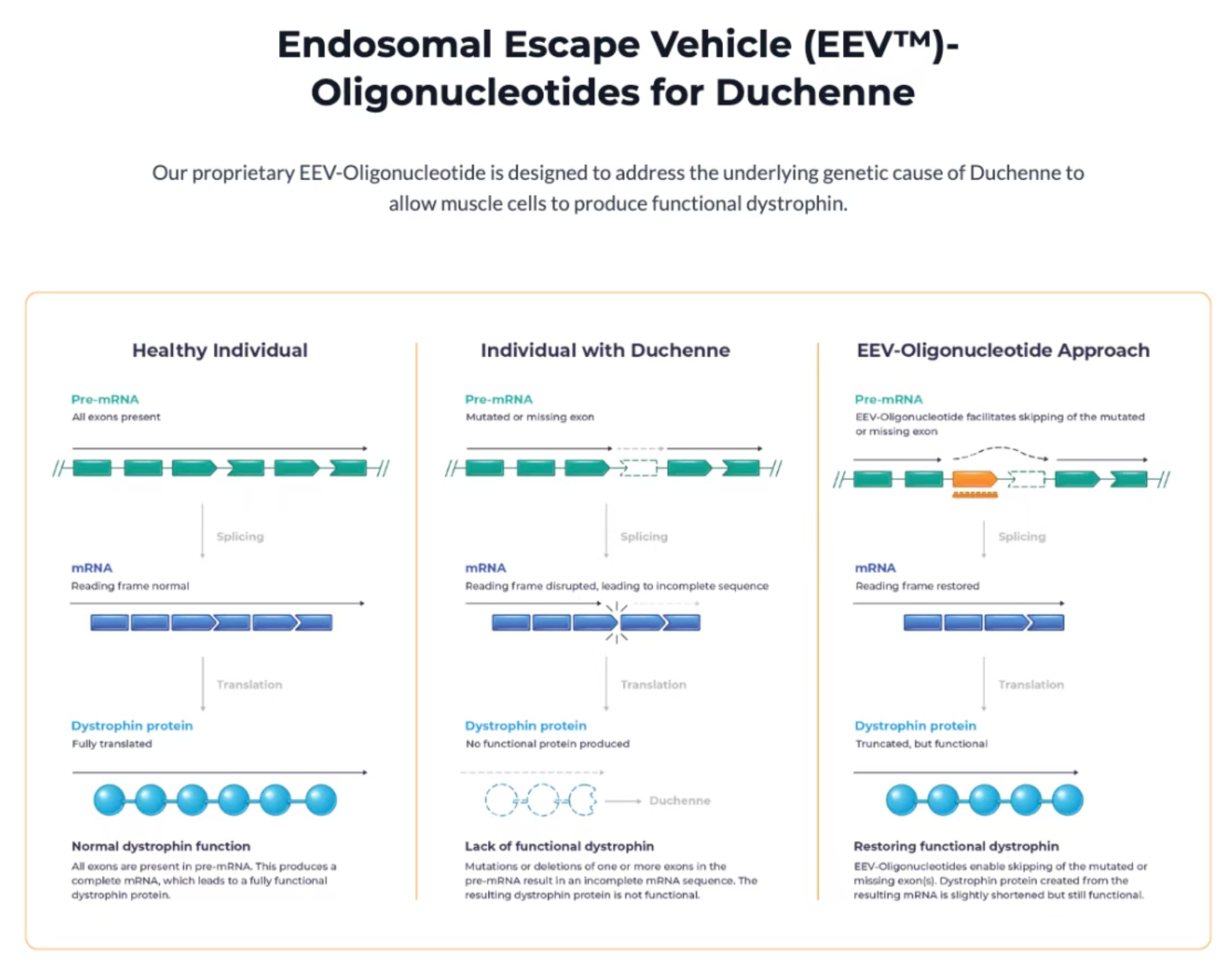
杜氏肌营养不良症(DMD)是一种由DMD基因突变引起的罕见遗传性肌肉退化疾病。由于缺乏负责维持肌肉细胞结构完整的抗肌萎缩蛋白(Dystrophin),患者的肌肉会逐渐丧失力量,最终往往因心力衰竭或呼吸并发症而早逝。
ENTR-601-44是Entrada开发的一款专有的内体逃逸载体(EEV)偶联寡核苷酸药物,专门针对携带适合“外显子44跳跃”基因突变的DMD患者(约占全球DMD患者的8%)。其核心机制是通过外显子跳跃,帮助细胞的剪接机器“跳过”有缺陷的外显子,从而产生较短但仍具备部分功能的抗肌萎缩蛋白。
临床数据
ELEVATE-44-201临床研究Cohort 1(第1队列,接受6 mg/kg剂量,由8名6-17岁患者组成)的数据亮点主要集中在两个方面:安全性和早期运动功能的改善。
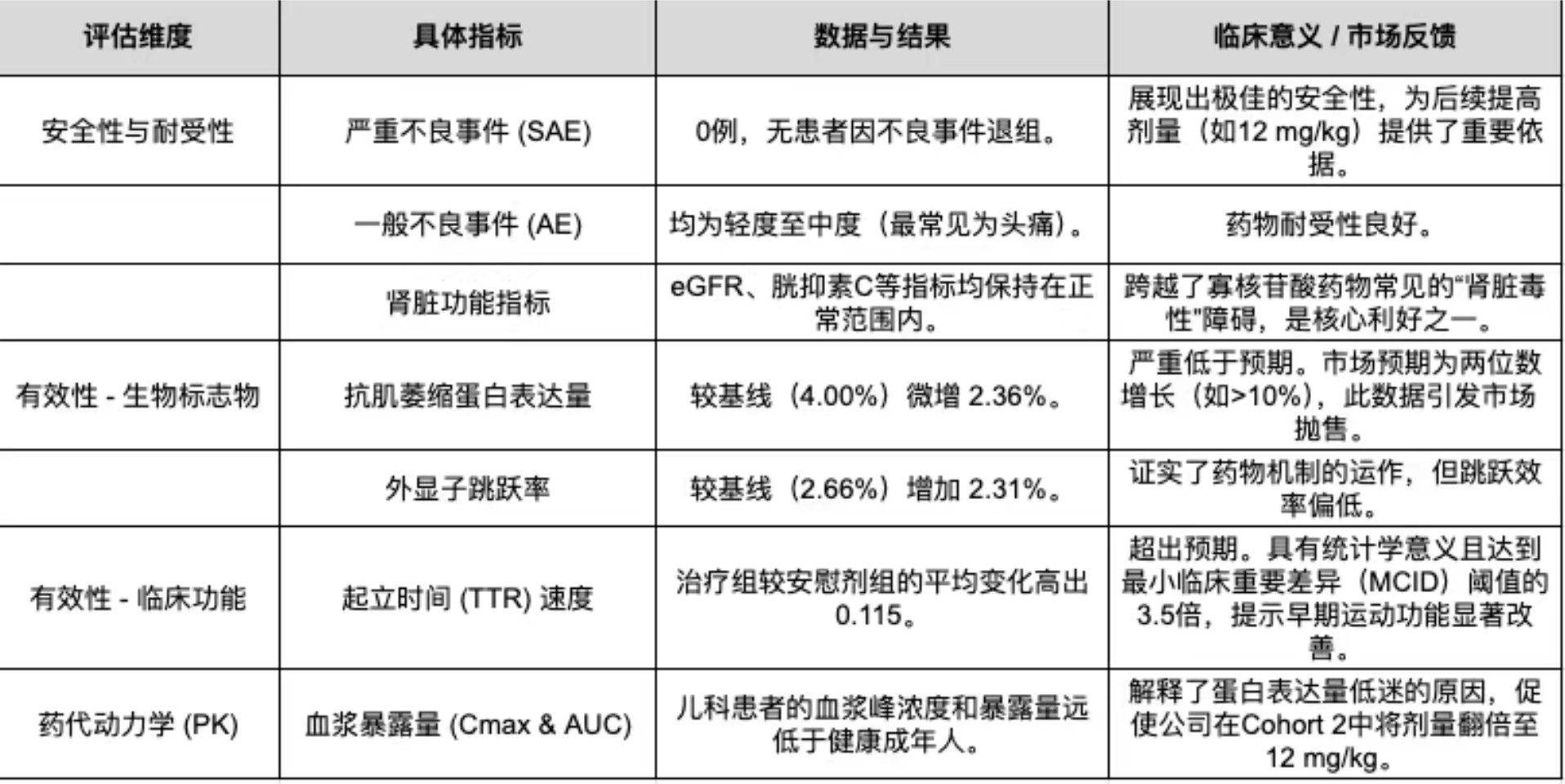
首先是“干净”的安全性数据。 在6 mg/kg的剂量下,没有出现严重不良事件(SAE),也没有患者因此退组。所有治疗期出现的不良事件均为轻度至中度(最常见的是头痛)。更重要的是,包括eGFR、胱抑素C等在内的肾功能指标均在正常范围内。对于寡核苷酸药物而言,肾脏毒性一直是个极难跨越的障碍,这份优异的安全耐受性数据无疑是个好消息。
其次是令人惊喜的早期功能改善。 尽管只是早期临床且用药时间短,但ENTR-601-44在“起立时间(Time to Rise, TTR)速度”这一关键的临床验证指标上,展现出了统计学上的显著改善。治疗组患者的TTR速度平均变化较安慰剂组高出0.115,这一数值是最小临床重要差异(MCID)阈值的3.5倍。公司高管表示,这种早期功能性指标的改善不仅出乎意料,且具有高度的临床意义。
抗肌萎缩蛋白的表达量:根据公布的数据,接受治疗的患者在给药六周后,其肌肉组织中的抗肌萎缩蛋白水平在基线4.00%的基础上,仅微弱增加了 2.36%。外显子跳跃率也仅在基线2.66%的基础上增加了2.31%。这一数据远远低于市场和公司的前期预期。投资银行William Blair的分析师指出,华尔街对该指标的基本预期是10%以上的增长,而Entrada管理层此前的指引也是“两位数的提升”。
如果没有对比,伤害可能还不会这么深。分析师指出,同赛道竞争对手Avidity Biosciences的寡核苷酸疗法del-zota在此前的读数中,治疗一年后抗肌萎缩蛋白增加了约25%(尽管两者并未进行严格的头对头比较)。在这个追求“Best-in-Class”的竞争赛道里,2.36%的个位数增幅显然难以让挑剔的资本买单。
数据偏差背后的原因:儿童与成人的药代动力学差异
面对大幅低于预期的蛋白表达量,Entrada给出了科学层面的解释:儿童患者与健康成人之间的药代动力学(PK)存在显著差异。
数据显示,Cohort 1中的儿科患者在接受给药后,其血浆药物峰浓度 Cmax 和血浆药物浓度-时间曲线下面积(AUC)均远低于此前的健康成年志愿者。Entrada首席执行官Dipal Doshi坦言最初看到这种差异时感到惊讶,但这一现象与公司近期获得的幼年非人灵长类动物(NHP)的数据高度一致。换言之,血浆暴露量不足导致了蛋白表达量的低迷。
展望
尽管遭遇了股市滑铁卢,但Entrada的临床进程并未中止。好消息是,Cohort 1展示出的极佳安全性,为后续提高剂量铺平了道路。目前,该研究已经启动了Cohort 2阶段,将给药剂量直接翻倍至 12 mg/kg。公司最新的PK模型预测,在12 mg/kg剂量下,血浆AUC将显著增加,从而大幅推高抗肌萎缩蛋白的表达水平。