背景与研究设计

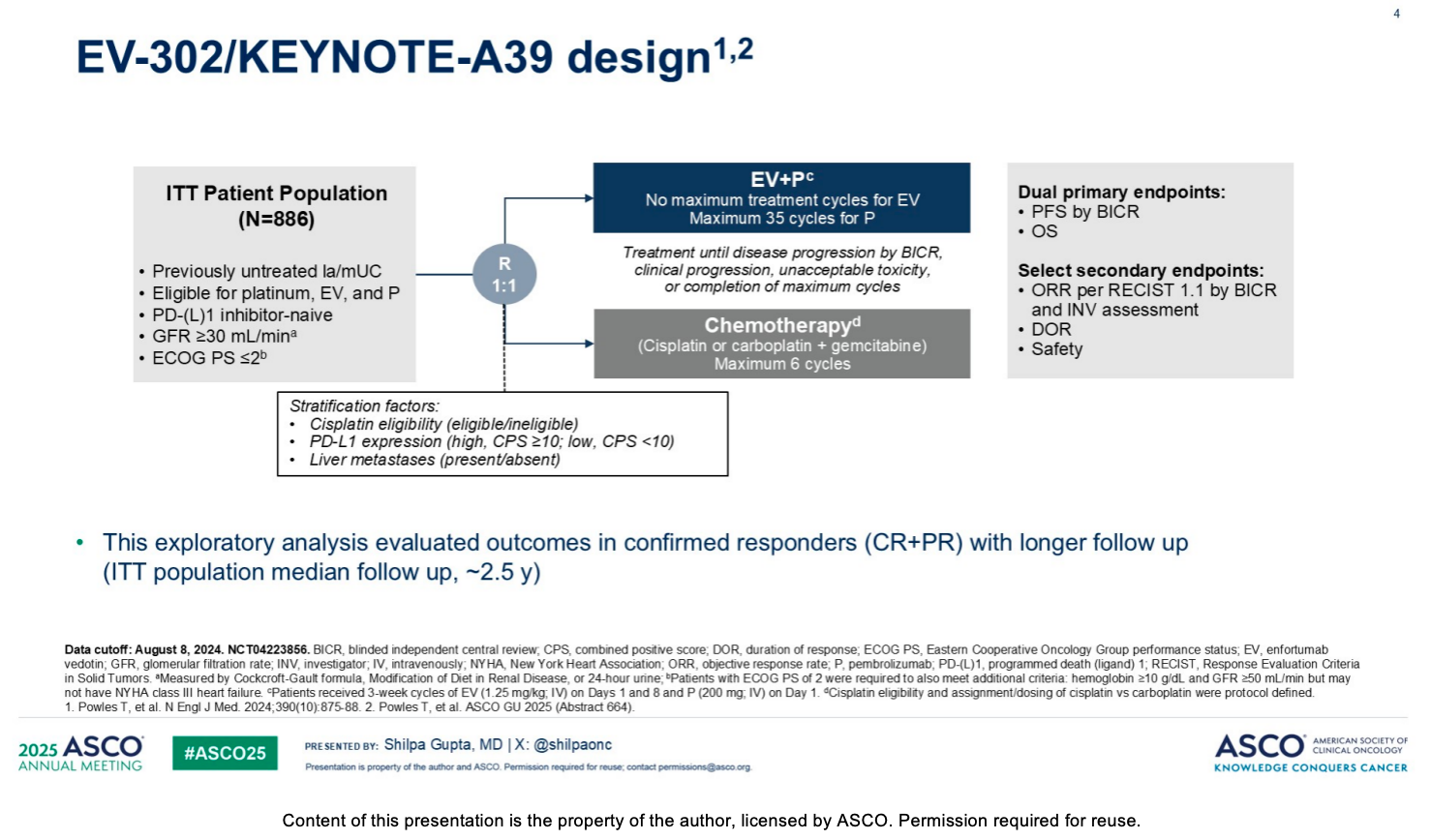
在针对既往未接受过治疗的局部晚期或转移性尿路上皮癌(la/mUC)患者的全局随机3期EV-302研究中,Enfortumab Vedotin(EV)联合帕博利珠单抗(P)已被确立为一线标准治疗方案 。
既往数据显示,在广泛的患者群体中,EV+P 的疗效显著优于含铂化疗,其客观中位无进展生存期(PFS)为 12.5 个月(化疗组为 6.3 个月),中位总生存期(OS)为 33.8 个月(化疗组为 15.9 个月) 。
此次更新的探索性分析聚焦于病情获得确认缓解的应答者(即达到完全缓解 CR 或部分缓解 PR 的患者),中位随访时间约为 2.5 年(29.1 个月) 。
研究采用1:1随机分组,评估 EV+P(无最大周期限制的EV,最多35个周期的P)对比最多6个周期的化疗
核心疗效数据与缓解率
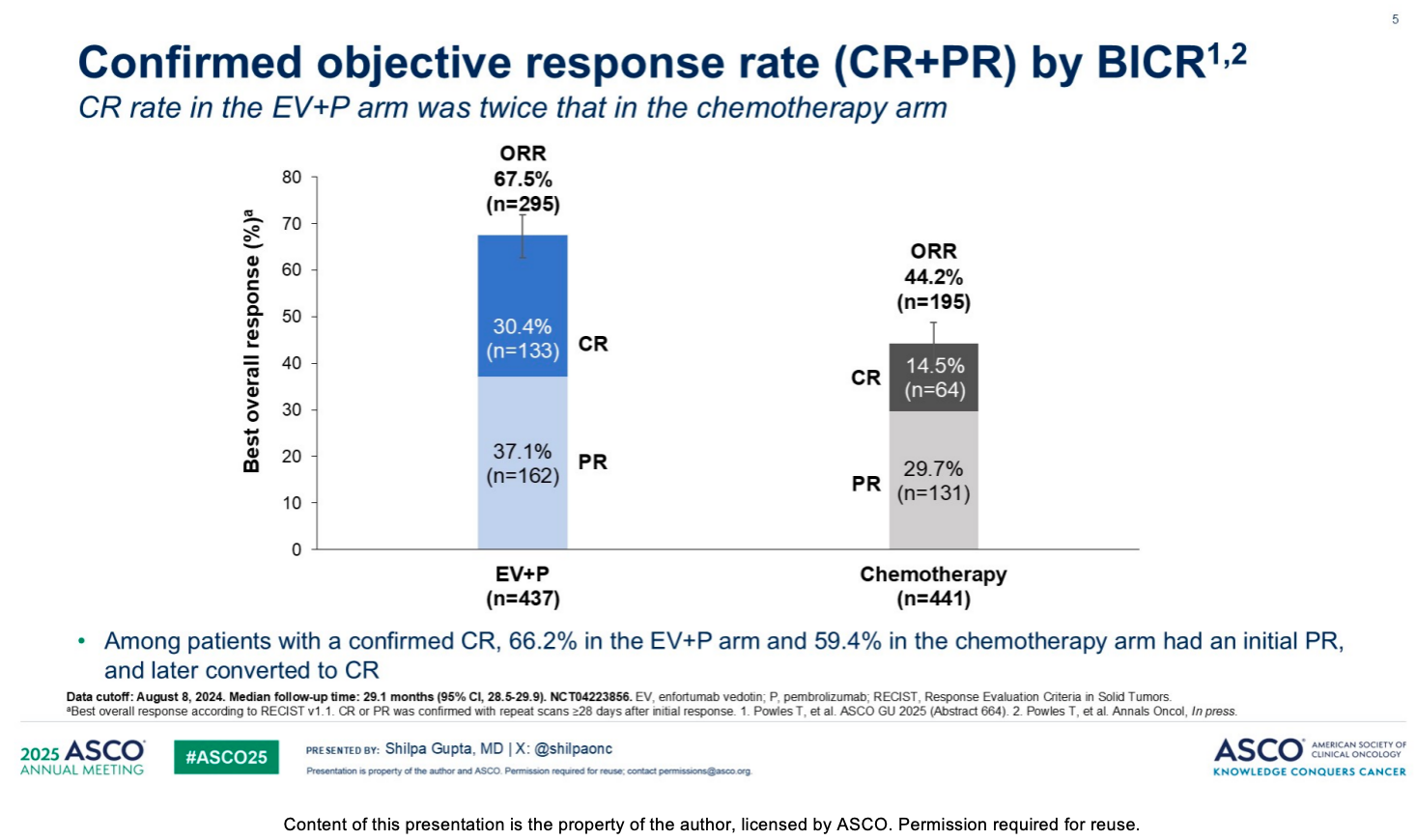
在获得缓解的患者中,EV+P 方案展现出了相较于传统化疗翻倍的深度缓解能力。
EV+P 组的客观缓解率(ORR)达到了 67.5%(n=295),而化疗组的 ORR 为 44.2%(n=195) 。
值得注意的是,EV+P 组的完全缓解(CR)率为 30.4%,是化疗组(14.5%)的两倍以上 。
在获得确认完全缓解(CR)的患者中,EV+P 组有 66.2% 的患者(化疗组为 59.4%)最初为部分缓解(PR),随后转化为完全缓解 。
无论在年龄(<65岁或≥65岁)、ECOG体能状态、原发肿瘤部位、转移类别(如内脏转移或仅淋巴结疾病)以及是否符合顺铂化疗条件等基线特征子组中,EV+P 组的应答者数量均多于化疗组 。
响应持续时间 (DOR)
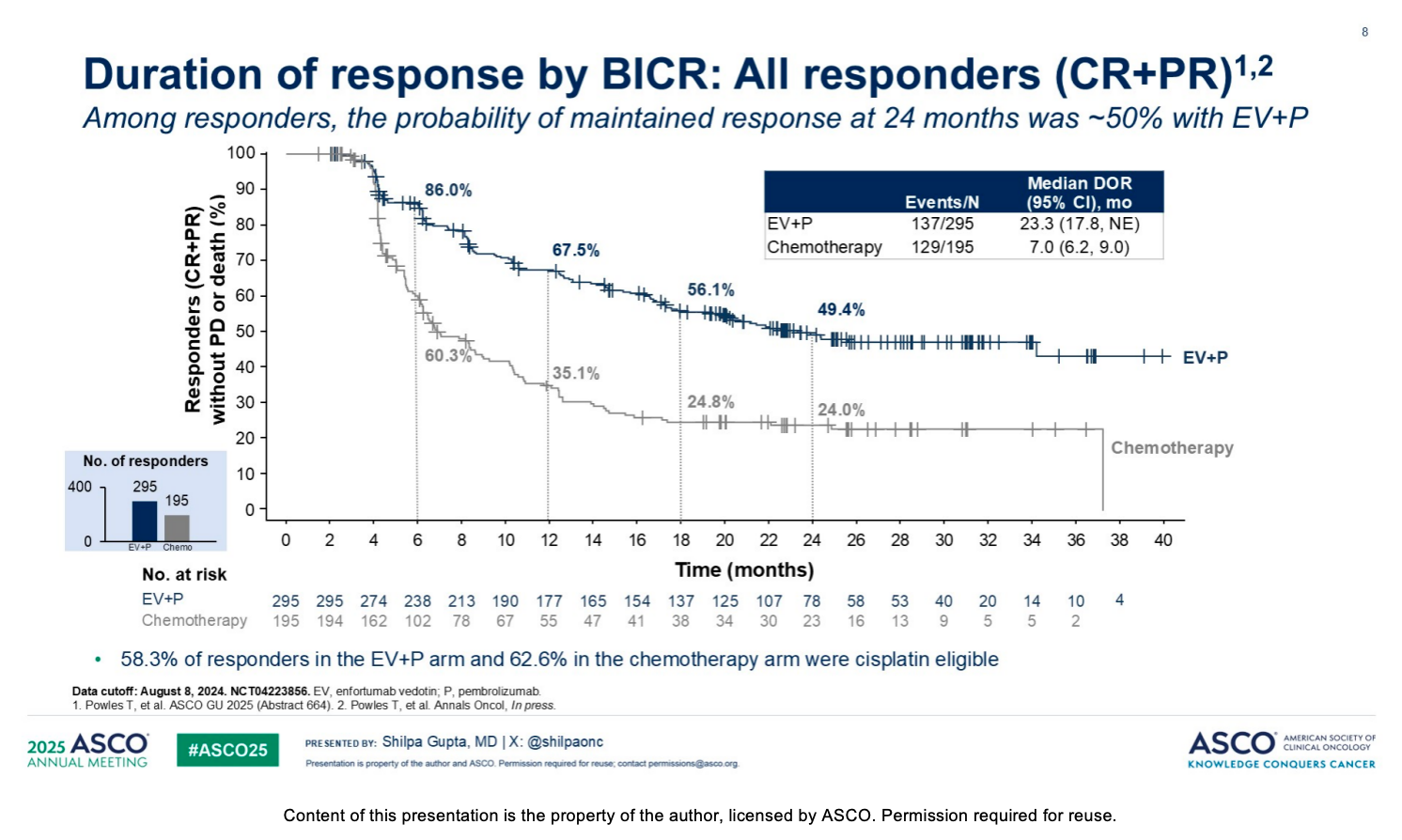
EV+P 方案不仅提高了缓解率,还显著延长了应答者的疾病控制时间。
独立中心审查委员会(BICR)评估显示,EV+P 组应答者的中位缓解持续时间(DOR)高达 23.3 个月,而化疗组仅为 7.0 个月 。
在 24 个月时,EV+P 组的应答者维持缓解状态的概率约为 50%(具体为 49.4%) 。
此外,达到完全缓解(CR)的患者对 EV+P 方案的响应具有高度持久性,在 24 个月时维持 CR 的概率高达 74% 。
安全性与剂量调整
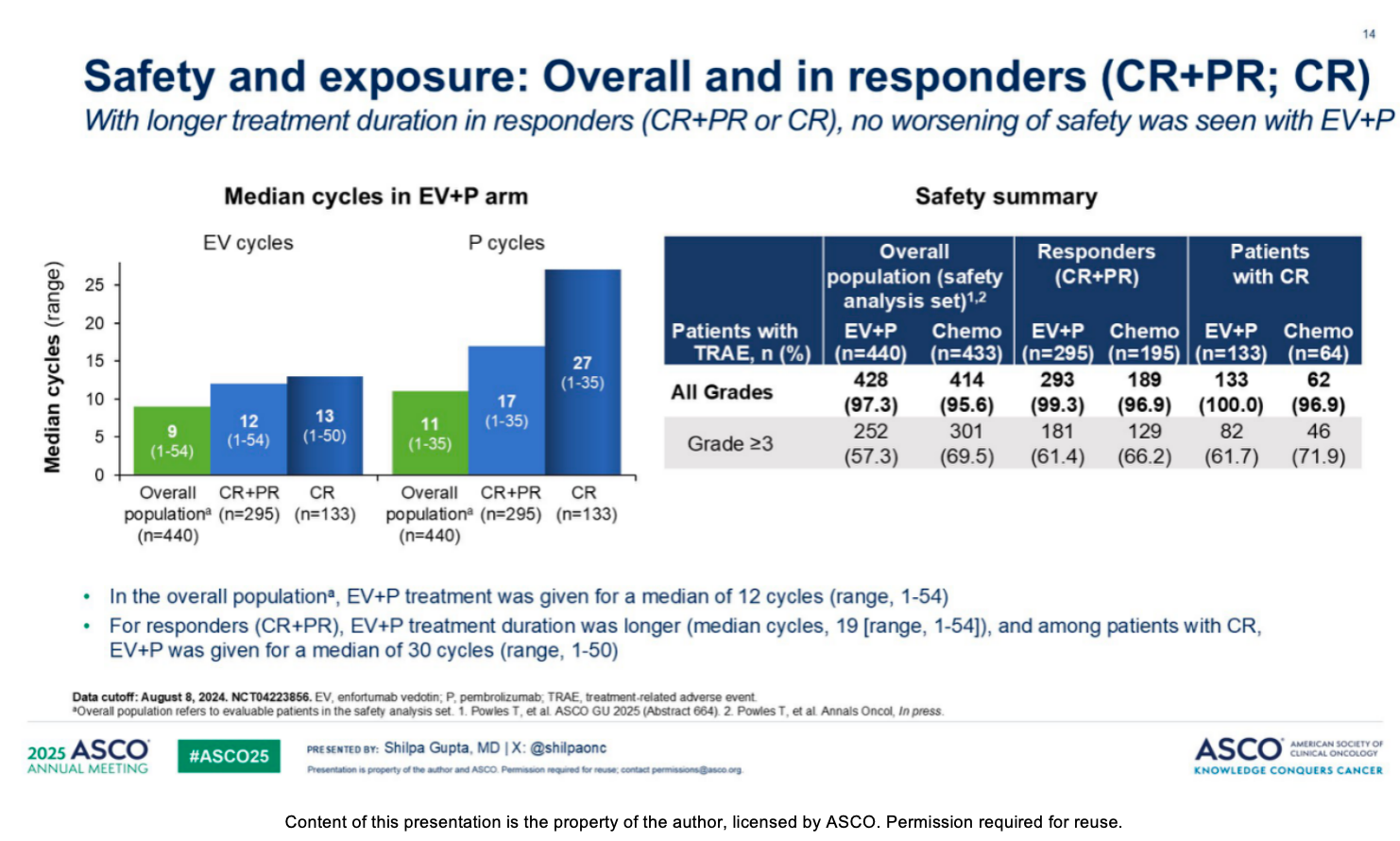
尽管获得缓解的患者接受了更长时间的治疗,但 EV+P 的整体安全性特征依然可控,且与总人群保持一致。
EV+P 组中,应答者的 EV 中位治疗持续时间为 9.7 个月(总人群为 7.1 个月),帕博利珠单抗的中位治疗持续时间为 13.2 个月(总人群为 8.5 个月)
EV 及帕博利珠单抗在应答者中的特别关注不良事件(如外周感觉神经病变、皮疹、严重皮肤反应、高血糖等)发生率及严重程度与总人群总体一致 。
由于治疗持续时间更长,应答者中因治疗相关不良事件(TRAE)导致的剂量调整更为常见 。其中 69.2% 的应答者经历了剂量中断(总人群为 59.8%),53.9% 经历了 EV 剂量减少(总人群为 43.0%) 。
适当的剂量调整和中断允许应答者继续接受治疗,从而在获得更多治疗周期的同时保持了安全的耐受性 。
结论
该探索性分析表明,在获得 CR 或 PR 的患者中,EV+P 相比化疗显著改善了生存结局 。EV+P 方案不仅具有比化疗高两倍的完全缓解率,且疗效持久 。这些数据进一步巩固了 EV+P 作为局部晚期或转移性尿路上皮癌一线标准治疗方案的地位,且该结论不受患者基线特征(包括顺铂耐受性)的影响 。