一、前言
FGF21R靶点药物在2025年迎来一波重磅交易和并购,总额超96亿美金,将这个曾经不被市场看好的靶点重新带入聚光灯下。
-
2025年5月,GSK以20亿美元(包括12亿美元首付款和8亿美金里程碑款)从Boston Pharma收购药物Efimosfermin alfa,一款每月一次皮下注射的FGF21类似物用于治疗严重肝病。
-
2025年9月,罗氏公司以35亿美元(包括24亿美元预付款,外加最高11亿美元的附条件价值权证)收购 89bio及其用于治疗中度至重度MASH(Metabolic dysfunction-associated steatohepatitis, 代谢功能障碍相关脂肪性肝炎,旧称NASH)的3期FGF21 类似物:Pegozafermin。
-
2025年10月,诺和诺德公司斥资52亿美元(包括47亿美元的预付款,外加5亿美元的附条件价值权证)收购Akero Therapeutics和其重要的资产FGF21类似物efruxifermin,治疗MASH,这将补充诺和诺德在基于 GLP-1 的代谢治疗领域的领导地位。
然而,FGF21R靶点的开发并不顺利,2021年9月,BMS因为FGF21类似物Pegbelfermin在关键临床未达到预期疗效而终止了对其开发,损失数亿美元的研发费用。
从2021年到2025年,到底发生了什么导致了曾经被不看好的赛道获得了如此大的升值?本报告将系统梳理FGF21的作用机理,市场定位、研发历史,关键临床,竞争格局,全球BD交易等方面,来整体梳理FGF21赛道的进展,并展望FGF21在日益拥挤的MASH治疗领域的未来竞争格局、组合疗法潜力和长期挑战。
二、作用机理
成纤维细胞生长因子21(Fibroblast Growth Factor 21,FGF21)是一种内分泌型成纤维生长因子(FGF)家族成员,主要由肝脏产生,也可能由脂肪组织、肌肉、胰腺等产生。
FGF21需要借助特定辅助因子受体β-Klotho (KLB)来激活FGFR1、2和3的"c"剪接同种型。β-Klotho是一种单通道跨膜蛋白,能够特异性识别FGF21并与FGFR形成受体复合物,从而介导信号传导。当β-Klotho缺失时,FGF21不能直接与FGFR结合,因此β-Klotho是介导FGF21生物学功能的关键因素。
FGF19 和 FGF21 可激活与必需辅助受体 KLB 结合的同型二聚体FGFR酪氨酸激酶。FGFR1/KLB激活的下游效应已得到充分研究,但 FGFR2/KLB和FGFR3/KLB的作用尚不清楚。FGF19 独特地激活FGFR4/KLB复合物,并引发与 FGF21 受体不同的下游效应。
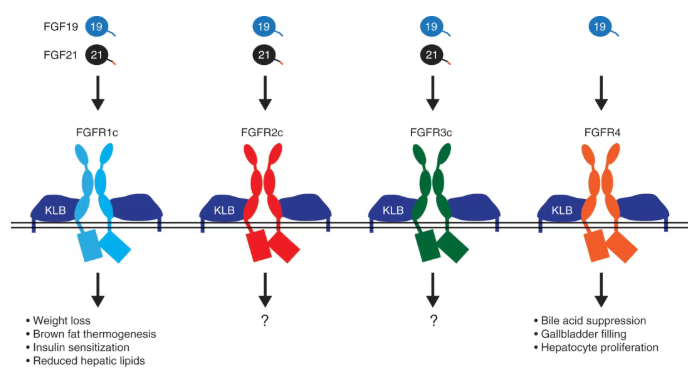
FGF21并非一个普通的生长因子,而是一种在代谢应激(如禁食)期间由肝脏分泌的内分泌激素。它像一位信使,向全身发出信号,指令身体启动一系列生存攸关的适应性反应:燃烧脂肪、提高胰岛素敏感性、抑制炎症。
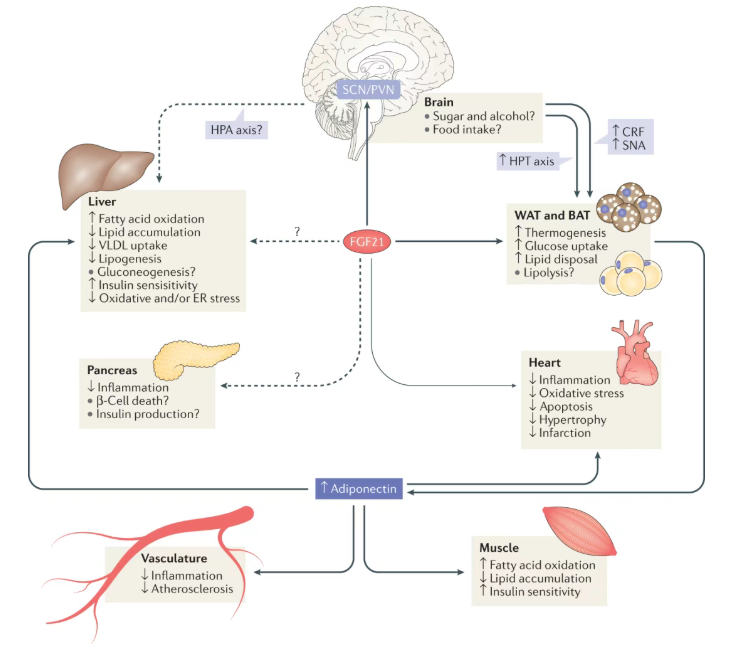
在肝脏中,FGF21直接促进肝脏脂肪含量的减少(减肝脂),并显著改善胰岛素敏感性,从而从源头上缓解肝细胞损伤。在脂肪组织中,它有效促进脂肪分解与能量消耗,有助于全面提升全身代谢健康水平。尤为重要的是,FGF21能够作用于中枢神经系统,调节食欲与能量偏好,显著降低对糖和酒精的渴望,这一机制与GLP-1类药物呈现出显著的协同效应。与主要聚焦减重和血糖的GLP-1不同,它不再是“头痛医头,脚痛医脚”的单靶点疗法,而是有望通过一个分子实体,系统性地解决代谢紊乱这一根本问题,展示出“一站式”解决方案的巨大潜力。
三、研发历史
3.1 第一代FGF21的失败
尽管FGF21的生物学机制令人神往,但将其转化为一种可行的药物却遇到了一个看似无法逾越的障碍。
药物代谢动力学局限
天然的FGF21蛋白有一个致命的缺陷:其在人体内的半衰期极短,大约只有30到60分钟。这意味着,要想维持有效的治疗浓度,患者可能需要持续静脉输注,这在临床上是完全不现实的。一个再强大的分子,如果无法在体内稳定存在,其治疗价值也等于零。这个药物代谢动力学(Pharmacokinetics, PK)上问题成为了第一代FGF21药物研发者必须攻克的首要难关。
最初的“补丁”:聚乙二醇化
为了延长FGF21的半衰期,各大公司不约而同地采用了当时最成熟、最普遍的蛋白质工程技术——聚乙二醇化(Pegylation)。这项技术通过将聚乙二醇(PEG)分子链连接到蛋白质上,增大其分子体积,从而减缓肾脏的清除速度,达到延长半衰期的目的。百时美施贵宝(BMS)的Pegbelfermin(BMS-986036)就是这一策略的典型代表。通过聚乙二醇化改造,Pegbelfermin的半衰期被成功延长,实现了每日或每周一次的给药频率,使其具备了临床开发的基本条件。
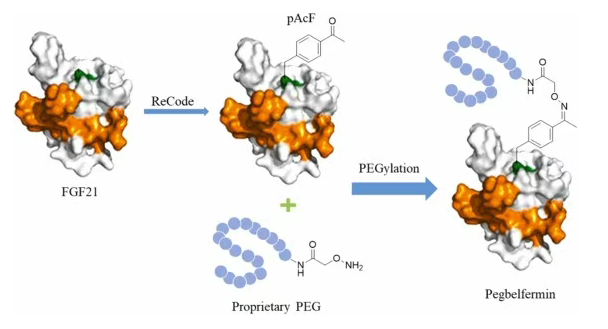
Pegbelfermin的临床失败
为了进一步验证pegbelfermin的疗效,BMS启动了名为FALCON的大型IIb期临床项目,该项目包括两项独立的关键性研究,旨在评估药物对MASH患者肝脏组织学的改善作用。
-
FALCON 1 (NCT03486899):该研究招募了197名经活检证实的、伴有进展期(F3期,即桥接样)肝纤维化的MASH患者。其主要终点设定在治疗24周时,评估一个复合终点:实现肝纤维化改善(至少改善1级)且MASH不恶化,或实现MASH缓解且纤维化不恶化。
-
FALCON 2 (NCT03486912):该研究则聚焦于病情更严重的患者,即伴有代偿期肝硬化(F4期)的MASH患者。其主要终点更为严格且更关注抗纤维化效果:在治疗48周时,实现肝纤维化改善(至少改善1级)且MASH不恶化。
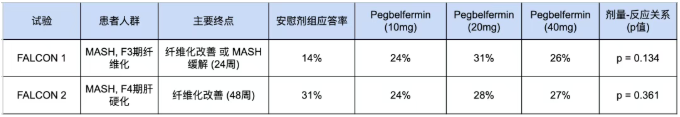
(表:FALCON1&2临床试验主要终点结果汇总)
如上表总结,FALCON项目的结果显示,Pegbelfermin未能证明其相对于安慰剂的明确优势,尤其是在关键的组织学终点上。
-
FALCON 1 结果: 该研究未能达到其主要终点。尽管在数值上,pegbelfermin治疗组(10mg, 20mg, 40mg)的应答率(24%-31%)高于安慰剂组(14%),但这种差异并未达到统计学显著性。更关键的是,研究未能观察到清晰的剂量-疗效关系(p=0.134),即更高剂量的药物并未带来更好的疗效。
-
FALCON 2 结果: 在肝硬化患者中的结果更为严峻。在治疗48周时,安慰剂组在主要终点上的应答率(31%)甚至在数值上高于所有pegbelfermin治疗组(24%-28%),同样没有显示出任何治疗获益(p=0.361)。
基于FALCON项目明确的负面结果,2021年11月,BMS正式宣布停止pegbelfermin的开发,其官方声明指出,研究结果“未能达到公司继续开发的门槛”。公司强调,这一决定是基于疗效不足,而非任何已观察到的安全性问题。
Pegbelfermin的失败不仅仅是疗效不足,更深层次地反映了第一代工程策略的根本局限性。简单的PEG化虽然成功延长了半衰期,但未能充分增强药物的内在效力或优化其与受体复合物的结合能力。FALCON 1试验中缺乏剂量-疗效关系是这一局限性的最关键证据。当40mg剂量组的疗效并不优于20mg剂量组时,这强烈表明简单地增加药物暴露量并不能带来更好的临床结果,药物的疗效已经达到了一个较低的“天花板”。这暗示了问题的根源在于分子本身的设计,而非剂量不足。它揭示了FGF21药物的开发不能仅仅满足于延长半衰期,而必须进行更根本的分子结构再造,以提升其生物学活性。这一教训为后来第二代药物的试验设计和数据解读提供了宝贵的经验。
3.2 新一代FGF21的崛起
第二代FGF21类似物的核心创新在于其分子结构的设计,旨在最大化药物与β-Klotho/FGFR受体复合物的结合亲和力和稳定性,从而产生更强、更持久的信号。
3.2.1 Efruxifermin (Akero/诺和诺德) - 双价优势
Efruxifermin(EFX)的技术核心是其双价Fc-FGF21融合蛋白的设计(如下图)。一个EFX分子包含两个经过改造的FGF21变体,它们通过一个人类IgG1的Fc片段连接在一起。这种双价结构(即每个分子有两个结合位点)能够产生“亲合力效应”(avidity effect)。当一个FGF21变体与细胞表面的受体复合物结合后,另一个FGF21变体能够更容易地与邻近的受体结合,从而极大地增加了整个分子与细胞表面的结合强度和稳定性。体外研究证实了这一优势:与单价类似物相比,EFX的结合强度(以解离常数Kd衡量)高出超过100倍,而其从受体上解离的速度则慢了30-40倍。这种卓越的受体结合特性是其强大生物学活性的根本原因,也是其与第一代PEG化药物的关键技术区别。
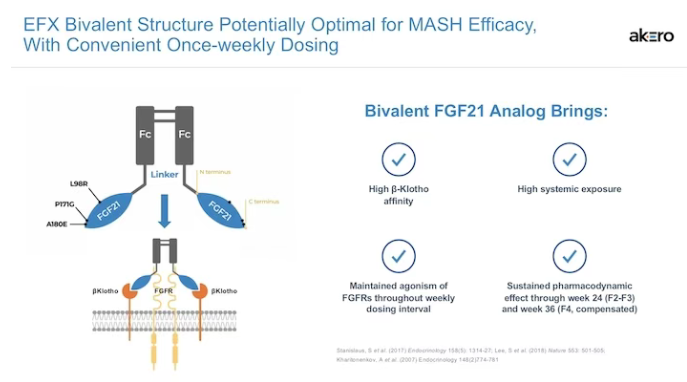
Efruxifermin临床:HARMONY试验
Efruxifermin在IIb期HARMONY研究(针对F2-F3期纤维化的MASH患者)中取得了里程碑式的成功,其结果重新验证了FGF21靶点的巨大潜力。在治疗24周时,50mg剂量组的数据如下:
-
41%的患者实现了肝纤维化改善至少1级,而安慰剂组为20%(p<0.05)。
-
高达76%的患者实现了MASH组织学缓解,而安慰剂组仅为15%(p<0.001)。
-
后续公布的96周长期数据显示,疗效持续增强,50mg剂量组中75%的患者实现了纤维化改善至少1级。
3.2.2 Pegozafermin (89bio/罗氏) - 优化的糖基化PEG修饰方法
Pegozafermin采用了另一种先进的工程技术——位点特异性糖基化PEG修饰。该技术通过在FGF21蛋白的特定位点引入一个糖基链,然后再将PEG分子连接到这个糖基链上。这种方法相比传统的随机PEG化,能够更精确地控制修饰位点,从而在延长半衰期(55-100小时)的同时,最大限度地保留蛋白质的天然生物学活性。
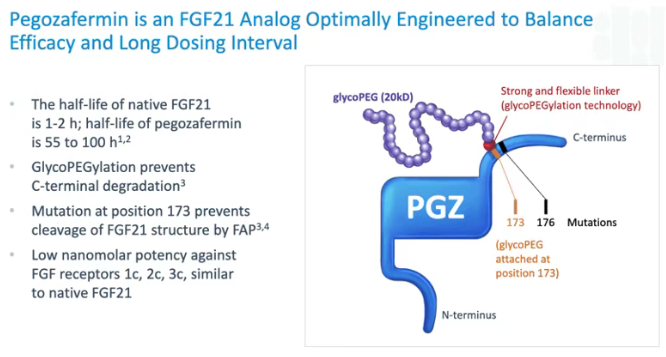
Pegozafermin临床: ENLIVEN试验
Pegozafermin同样在IIb期ENLIVEN研究(针对F2-F3期MASH患者)中取得了令人信服的阳性结果。在治疗24周时,44mg 每两周一次的给药方案达到了所有主要和次要终点:
-
27%的患者实现了肝纤维化改善至少1级,而安慰剂组仅为7%(p=0.008)。
-
26%的患者实现了MASH组织学缓解,而安慰剂组仅为2%(p=0.0005)。
-
药物在48周时显示出持续的疗效,并且在已经接受GLP-1药物治疗的患者中同样有效。
3.2.3 Efimosfermin (Boston Pharma/GSK) - 剂量与便利性的视角
Efimosfermin是一种长效FGF21变体,通过与人IgG1的Fc片段融合而构建。其工程设计的重点在于提高热力学稳定性和延长半衰期,最终实现了每月一次的皮下注射给药方案。这一给药频率在慢性病治疗中具有显著的商业优势,能极大提高患者的依从性。
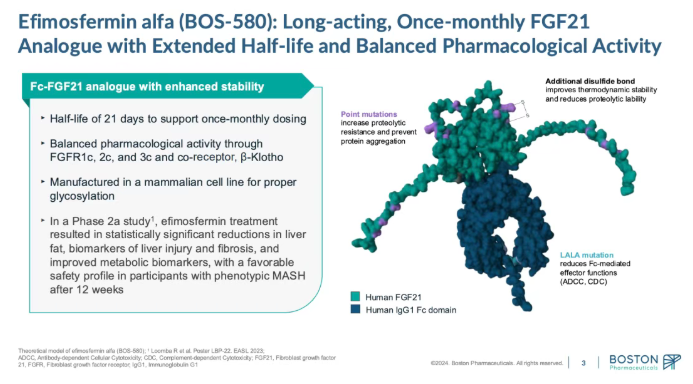
Efimosfermin 的II期临床
在一项针对F2-F3期MASH患者的II期研究中,300mg每月一次的efimosfermin在治疗24周后显示出统计学显著的疗效:
-
45.2%的患者实现了肝纤维化改善至少1级,而安慰剂组为20.6%(p=0.038)。
-
67.7%的患者实现了MASH组织学缓解,而安慰剂组为29.4%(p<0.01)。
综上所述,以上三个案例清晰地展示了第二代FGF21类似物如何通过不同的工程策略实现了临床成功,头对头比较如下表。
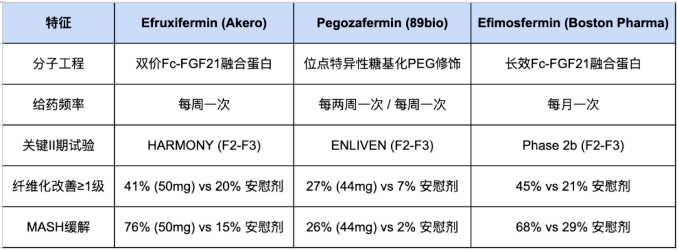
四、FGF21在MASH疾病治疗中的定位
MASH市场潜力巨大。据估计,2024年全球MASH患病人数约为3.5亿。受此驱动,预计到2030-2033年,全球MASH治疗市场规模将超过300亿美元,这是一个足以容纳多个重磅炸弹药物的广阔市场。随着MASH治疗领域首款药物Rezdiffra的获批以及多款后期在研药物的涌现,FGF21类似物必须在一个日益拥挤和复杂的竞争环境中找到自己的精准定位。
4.1 与竞争机制的基准比较
-
vs. 甲状腺激素受体-β (THR-β) 激动剂 (Rezdiffra/Resmetirom): Madrigal公司的Rezdiffra是首个获FDA批准用于治疗MASH的药物。然而,其疗效被认为是中等水平:在关键的MAESTRO-NASH试验中,实现纤维化改善(≥1级)的患者比例约为26%,而安慰剂组为14%,安慰剂校正后的净获益约为12%。同时,Rezdiffra也伴有胃肠道副作用。多项网络荟萃分析表明,FGF21类似物在MASH消解和纤维化改善这两个关键组织学终点上的疗效均优于THR-β激动剂。因此,FGF21类药物的定位是疗效更优的注射类药物,而Rezdiffra则凭借其口服便利性占据特定市场。
-
vs. GLP-1单药激动剂 (司美格鲁肽): 以司美格鲁肽为代表的GLP-1类药物,凭借其强大的减重效果,在MASH消解方面表现出色,应答率可达59%-63%。然而,其对肝纤维化的直接改善作用相对温和,安慰剂校正后的净获益率约为14.5%。这凸显了FGF21类药物的核心优势:更直接、更强效的抗纤维化作用。GLP-1主要通过改善上游的代谢驱动因素(如肥胖和胰岛素抵抗)来间接影响肝脏,而FGF21则能直接作用于肝脏,抑制纤维化进程。
下表直观地比较了不同机制药物在MASH (F2-F3期) 关键组织学终点上的疗效。
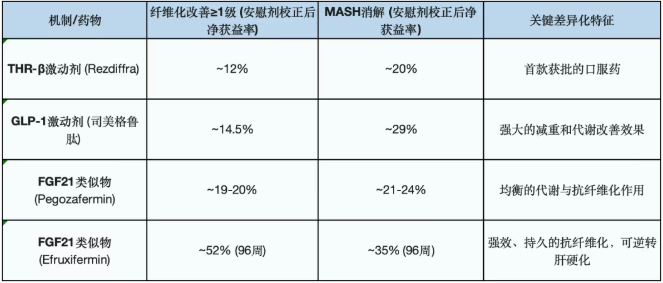
4.2 患者分层与未来市场细分
综合以上比较,未来的MASH市场不太可能出现“赢家通吃”的局面,而将是一个根据疾病严重程度和患者临床表型进行精细化分层的市场。
-
“代谢型”MASH患者: 对于以肥胖、2型糖尿病等代谢紊乱为主要特征,且肝纤维化程度较轻(F1-F2期)的患者,基于GLP-1的疗法(包括单药和多靶点激动剂)将可能成为一线首选。这些药物能从根本上解决驱动疾病进展的代谢引擎,并可能使部分患者的肝脏病理得到缓解。
-
“纤维化型”MASH患者: 对于肝纤维化已进展至中晚期(F3-F4期)的患者,FGF21类似物将成为治疗方案的核心。在这部分患者中,单纯的减重和代谢改善可能不足以逆转已经形成的肝脏结构性损伤。FGF21类药物强大的直接抗纤维化作用使其成为不可或缺的治疗选择。最常见的治疗模式将是与GLP-1类药物联合使用,以同时控制代谢驱动因素和逆转肝纤维化。对于无法耐受GLP-1或代谢控制良好的患者,FGF21单药治疗也可能是一种选择。
-
偏好口服治疗的患者: 对于拒绝注射治疗或因其他原因不适合使用注射药物的患者,Rezdiffra作为目前唯一的口服选择,将占据一个重要的细分市场。
五、竞争格局
5.1 概述
FGF21的治疗前景在经历了多年的探索和挫折后,正迎来一个决定性的复兴时期,制药巨头纷纷布局。如下表所列,全球FGF21研发管线总共44条,其中在研管线32条。
在FGF21单药治疗的后期开发阶段(Phase 3),竞争格局呈现“双雄争霸”:89bio公司(被罗氏收购)的Pegozafermin和Akero Therapeutics(已被诺和诺德收购)的Efruxifermin。这两种药物展现出差异化的临床特征:Pegozafermin以其在肝脏和全身代谢方面的“均衡代谢”优势而著称,而Efruxifermin则凭借其强大的、甚至可逆转肝硬化的“纤维化优先”疗效脱颖而出。
中国公司在FGF21赛道呈现出快速跟进和多靶点创新上,总共14条在研管线正在推进。安源医药和正大天晴正在联合推进其长效FGF21-Fc融合蛋白药物AP-025(TQA2225)的国内临床2期治疗非酒精性脂肪性肝炎(NASH)试验;中国公司更多的布局显著地集中在开发多靶点激动剂上。如上海民为生物的FGF21R x GIPR x GLP-1R三激动剂MWN-105,目前针对肥胖进行国内2期临床,同时针对MASH获得美国FDA的临床许可(2025年1月);东阳光药业的GLP-1/FGF21双靶点药物HEC88473正在针对2型糖尿病、非酒精性脂肪性肝炎、肥胖症开展2期临床;它们的核心思路是将FGF21与其他关键的代谢调节激素(主要是GLP-1,有时还包括胰高血糖素GCGR)的作用机制整合到一个分子中。
另外,浙江道尔生物、北京质肽生物、天士力、北京吉源生物、鸿运华宁、北京志道生物、北京因诺惟康都在这个赛道布局。完整竞争格局如下表所示。
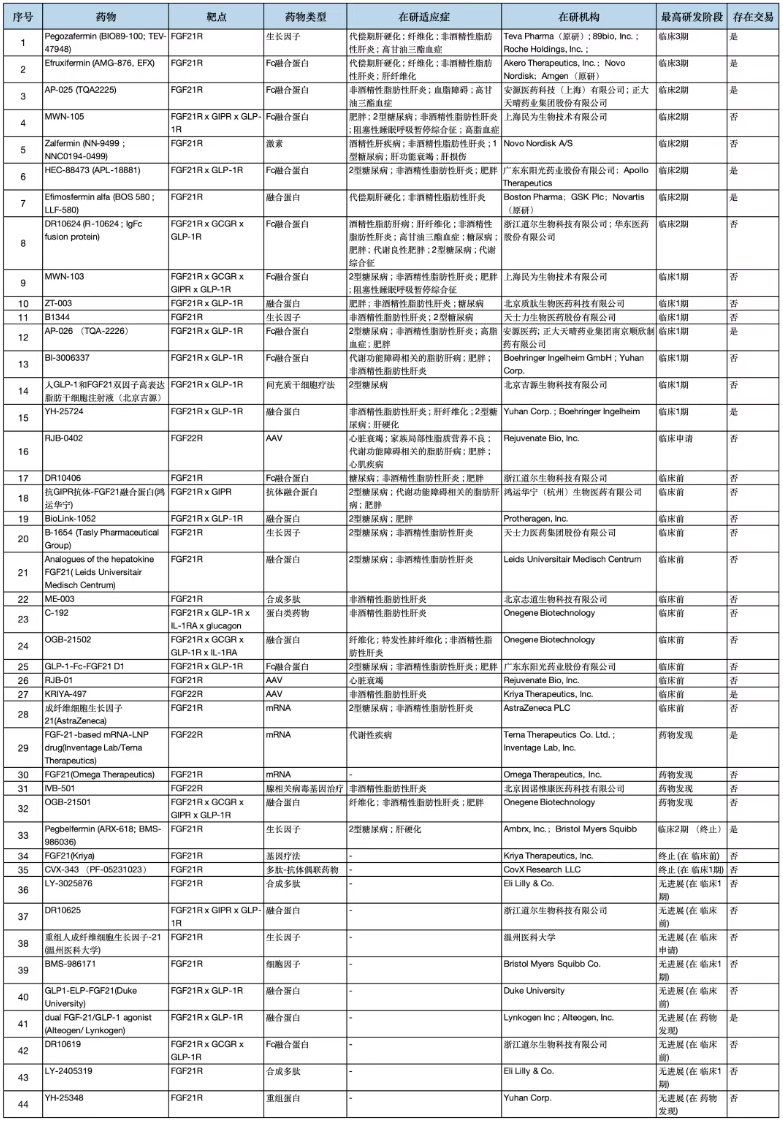
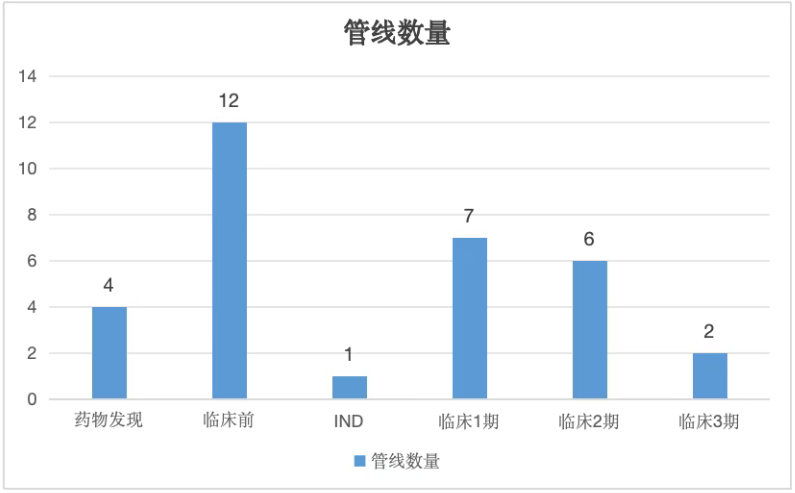
目前在研管线32条,不同阶段分布如下图。Efruxifermin在2023年底在全球启动多项针对MASH的临床三期试验SYNCHRONY;Pegozafermin在2024年3月宣布启动针对MASH的3期 ENLIGHTEN-Fibrosis 临床试验;其他大部分集中在1期和2期临床和临床前研究,随着竞争的加剧,会有更多的管线陆续披露。
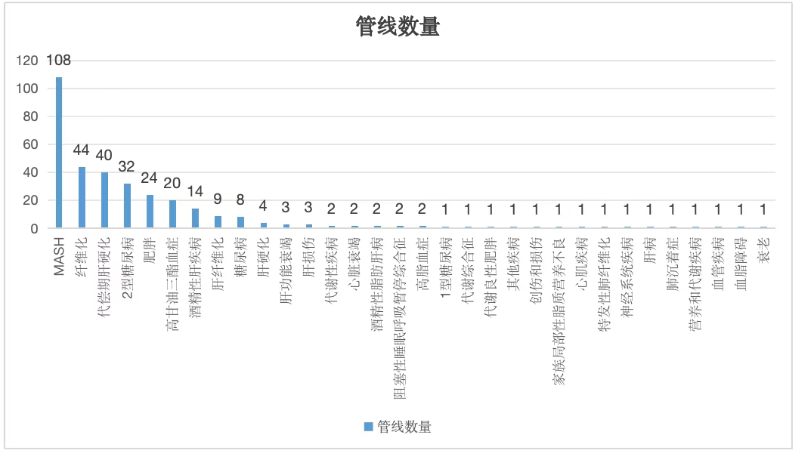
FGF21管线的疾病分布如下图,主要集中在MASH等严重肝病,其他相关疾病如2型糖尿病、肥胖、高甘油三酯血症也在被广泛研究。
5.2 新兴技术
在工程化蛋白药物和多靶点激动剂激烈竞争的同时,更具颠覆性的下一代疗法正在兴起,它们有望从根本上改变MASH等慢性代谢病的治疗模式。
基于腺相关病毒 (AAV) 的基因疗法:有望一次性治愈
Kriya Therapeutics公司的KRIYA-497就是该领域的代表。临床前研究显示,单次肌肉注射AAV-FGF21可以在动物模型中实现对肝纤维化的持久逆转,并预防肝细胞癌的发生。这种“一次性治疗”的潜力是革命性的。然而,AAV基因疗法也面临着巨大的挑战,包括潜在的免疫原性(预存抗体可能导致治疗无效)、长期安全性(如整合致瘤风险)、复杂的生产工艺和极高的治疗成本,这些因素目前限制了其在MASH这类广泛人群慢性病中的应用前景。
mRNA疗法:一种瞬时但可能更安全的方法
mRNA疗法利用脂质纳米颗粒 (LNP) 将编码FGF21的mRNA分子递送至体内细胞,利用细胞自身的翻译机制产生FGF21蛋白。与AAV不同,mRNA不会整合到宿主基因组中,理论上安全性更高。临床前研究表明,皮下注射FGF21 mRNA能够有效逆转小鼠的肥胖、胰岛素抵抗和肝脂肪变性。然而,mRNA的作用是瞬时的,需要重复给药,这使其在便利性上与长效蛋白类似物相比并无优势,更像是现有注射疗法的一种替代形式,而非颠覆性技术。
六、BD交易
目前公开的关于FGF21赛道相关交易如下表,总共15笔交易,披露总额超过108亿,基本都发生在2025年。
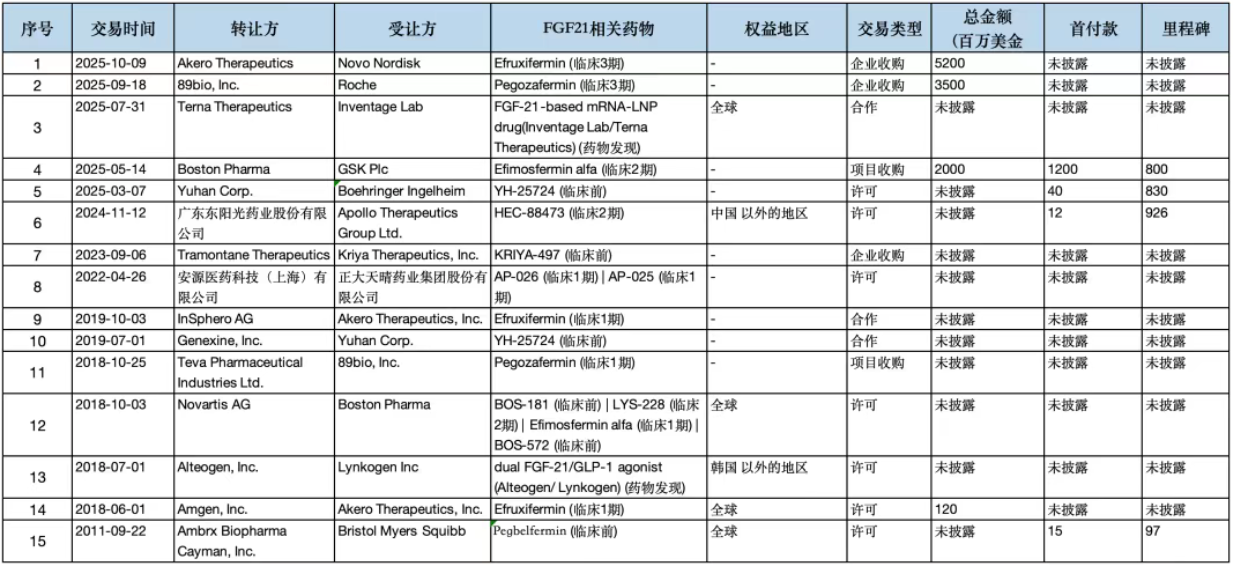
2025年5月,GSK以20亿美金总额(包括12亿美元预付款和8亿美元的里程碑)收购了Boston Pharma的Efimosfermin alfa。
2025年9月,制药巨头罗氏宣布以35亿美金总额(包括24亿美元预付款,外加最高11亿美元的附条件价值权证)收购89bio,获得Pegozafermin管线。行业分析师预测pegozafermin的全球销售峰值可达47亿美元,具有成为重磅炸弹药物的潜力。
2025年10月,代谢疾病领域的巨头诺和诺德宣布以52亿美金总额(包括47亿美元的预付款,外加5亿美元的附条件价值权证)收购Akero Therapeutics,从而获得管线Efruxifermin。该药物能够与诺和诺德强大的GLP-1受体激动剂产品线(如Wegovy)形成强大的协同效应,为未来开发针对MASH的组合疗法提供了可能,通过饱腹感(GLP-1)和能量消耗(FGF21)的双重机制进行干预。
七、总结
FGF21的研发故事充分展现了制药创新的魅力,有力地证明了科学的坚韧和技术的创新如何能够将一个濒临失败的治疗方案重新带回舞台中央。在未来的竞争中,长期的安全性数据、与GLP-1激动剂的组合策略,以及在日益拥挤的市场中的差异化定位。