5月11日,美国临床阶段生物技术公司Fractyl Health宣布,荷兰监管机构已授权其核心管线 RJVA-001 启动1/2期首次人体临床试验。成为全球首个步入临床开发阶段的2型糖尿病(T2D)基因疗法,通过将GLP-1基因靶向递送至胰腺,有望实现代谢疾病的“一次性长期缓解”。
公司预计2026年下半年完成第一例患者给药,并同时推进基因疗法在肥胖治疗中的进程。
作用机制与临床试验设计
1. 创新MOA:Rejuva® Smart GLP-1™ 平台与局部递送技术
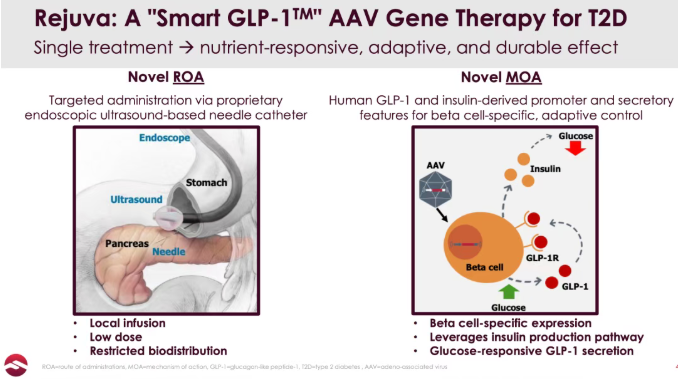
对于新药研发专家而言,将AAV基因疗法应用于受众极广的慢性代谢疾病,最大的技术挑战在于靶向性与系统性毒性。 RJVA-001基于Fractyl独有的Rejuva平台开发。其给药路径并未采用传统的静脉输注,而是创新性地利用内镜超声引导(EUS)直接将药物递送至胰腺。这种局部给药方式大幅降低了AAV在肝脏等非靶器官的系统性暴露,提升了安全性。 在机制上,RJVA-001特异性靶向胰岛β细胞,通过载体基因重组,使胰岛细胞自身获得合成并分泌GLP-1激素的能力。更重要的是,它的启动子经过特殊设计,能够在患者进食后产生生理性、脉冲式的GLP-1释放(Smart GLP-1),模拟人体天然的激素调节途径,这与目前通过外源性系统给药带来持续超生理浓度的GLP-1RAs有着本质区别。

2. 1/2期首次人体试验(FIH)设计
-
试验类型:开放标签、多中心、单次剂量递增(SAD)试验。
-
目标人群:年龄35-70岁,BMI 27-40 kg/m²,且在使用包括GLP-1RAs及最多三种非胰岛素口服降糖药后,血糖控制仍不佳(HbA1c介于7.0%-10.0%之间)的T2D成年患者。
-
剂量与队列:包含3个递增剂量组(每组3人),随后是一个最多包含20名患者的扩展队列。
-
临床终点:患者将接受为期12个月的主要随访,以评估药物的安全性、耐受性、血糖控制水平、免疫反应及胰岛β细胞功能,同时还将进行长达5年的长期随访,以验证基因疗法的持久性。
里程碑意义
1. 开启慢病基因治疗
以往,基因疗法(Gene Therapy)往往被局限于罕见病、单基因突变疾病(如SMA、血友病)以及肿瘤学领域。RJVA-001成为全球首个进入临床阶段的T2D AAV基因疗法,标志着基因编辑/递送技术正式向具有数亿患者基础的复杂代谢慢病进军。若该路线被验证成功,代谢疾病的治疗将从“慢性病终身症状管理”跃升至“器官水平的单次疾病修饰(Disease-modifying)”,彻底解决患者依从性差的难题。
2. 确立Fractyl Health的“双重临床阶段”地位
此次获批对Fractyl Health公司自身意义重大。目前公司拥有两大核心平台:
-
Revita®(十二指肠粘膜表面重建术): 正在进行用于GLP-1停药后体重维持的关键性临床(REMAIN-1)。
-
Rejuva®(胰腺基因疗法): 随着RJVA-001进入临床,Fractyl正式转型为拥有两款处于临床阶段的创新代谢疾病治疗公司。这一里程碑极大地丰富了公司的资产组合,并显著提升了其在MNC(跨国药企)合作中的估值溢价能力。
展望
随着荷兰临床申请(CTA)的获批,Fractyl Health制定了密集且充满雄心的下一步推进计划:
-
临床推进与数据读取:公司计划在2026年下半年完成RJVA-001首例患者的给药(取决于临床中心的启动进度),并预期在同年下半年公布首批初步临床数据(Preliminary Data)。
-
全球多中心扩张:公司已同步向澳大利亚监管机构提交了临床试验申请,预计将在2026年第三季度获得澳大利亚的监管反馈,以加速亚太地区及全球范围的临床部署。
-
下一代管线开发(减重靶点前推):除了针对T2D的RJVA-001外,其Rejuva平台还有后续的强劲弹药。公司正积极推进RJVA-002的临床前研究,这是一款被设计为双重GIP/GLP-1激动剂的AAV基因疗法,其适应症将直接剑指目前大热的“肥胖症”市场。