随着礼来的口服GLP-1药物Orforglipron的审批,全球减肥药战场已经从注射用药拓展到口服领域,GLP-1药物的临床开发与商业化竞争已进入全面白热化的阶段。目前市面上最火的两款药物:
-
诺和诺德的口服版Wegovy(司美格鲁肽),于2025年12月获得美国食品药品监督管理局(FDA)批准用于肥胖治疗。 -
礼来的Orforglipron则紧随其后,借助FDA创新的“国家优先审查凭证”(CNPV)试点计划通道,在短短50天内于2026年4月初以商品名Foundayo获得闪电批准。
本文将立足于以上两款口服减肥药的核心临床:OASIS-1、OASIS-4和ATTAIN-1 三期临床试验原始数据,对口服司美格鲁肽与Orforglipron在疗效上限、安全耐受性、药代动力学特性、现实世界依从性及未来商业化前景等维度进行对比与剖析。
核心临床对比概览
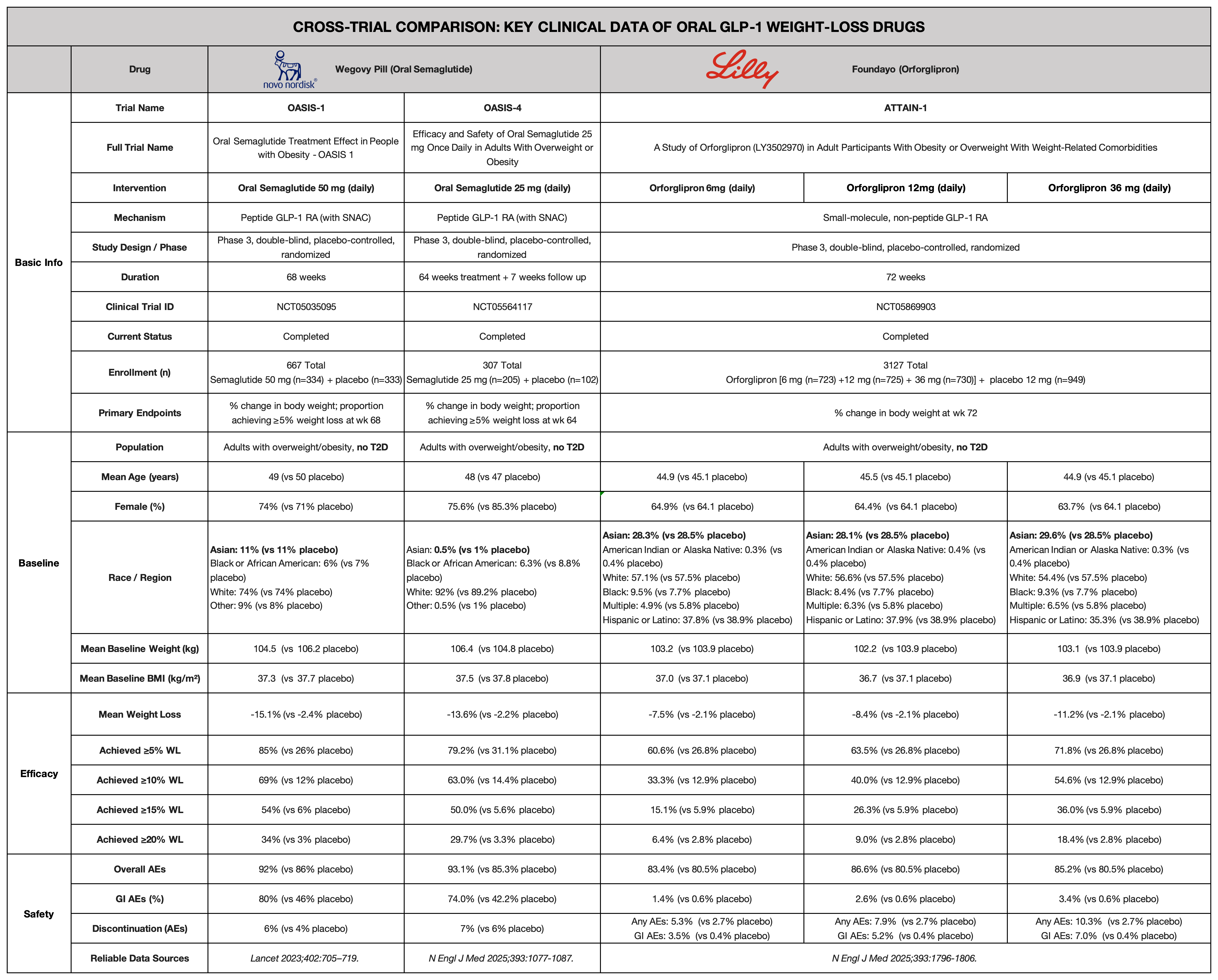
核心临床试验的选择考量
上述三项关键三期临床试验均采用了多中心、随机、双盲、安慰剂对照设计;且针对不伴随糖尿病的超重或肥胖人群;所有参与者在接受药物干预的同时,均需接受标准化的生活方式干预(通常包括每日减少500千卡热量摄入的饮食指导以及每周至少150分钟的体力活动建议) 。
入组标准在各项试验中保持了高度的同质性:均要求参与者为成年人( >= 18岁),体重指数(BMI)>= 30kg/m^2(肥胖),或者BMI >= 27 kg/m^2(超重),且至少伴有一种与体重相关的合并症(如高血压、血脂异常、阻塞性睡眠呼吸暂停或心血管疾病),且明确排除了既往已确诊为1型或2型糖尿病的患者,同时要求患者近期有记录的饮食减重失败史。
-
OASIS-1 试验: 旨在评估极高剂量50 mg口服司美格鲁肽的疗效。试验为期68周,共入组667名患者,以1:1的比例随机分配至司美格鲁肽50 mg组(n=334)或安慰剂组(n=333)。药物从3 mg起始,每4周进行一次剂量递增(3 mg -> 7 mg -> 14 mg -> 25 mg),最终在第16周达到50 mg的维持剂量。
-
OASIS-4 试验: 旨在评估更具普适性与耐受性平衡的25 mg口服司美格鲁肽。试验包括64周的治疗期和7周的随访期(总周期71周),共入组307名患者,以2:1的比例随机分配至司美格鲁肽25 mg组(n=205)或安慰剂组(n=102)。剂量递增同样每4周进行一次(3 mg -> 7 mg -> 14 mg),在第12周达到25 mg维持剂量。
-
ATTAIN-1 试验: 旨在全面评估小分子药物Orforglipron不同剂量梯度的疗效。这是一项规模宏大的试验,为期72周,共入组高达3127名患者。患者以3:3:3:4的比例随机分配至Orforglipron 6 mg组(n=723)、12 mg组(n=725)、36 mg组(n=730)或安慰剂组(n=949)。36 mg高剂量组的滴定周期更长,从1 mg起始,每4周递增,分别在第8周达到6 mg,第12周达到12 mg,直至第20周才达到36 mg的最终靶剂量。这种更为缓慢的延长滴定期设计,深刻反映了研究团队对其潜在胃肠道不良反应的预判与预防策略。
基线对比洞察
-
年龄与性别偏移: ATTAIN-1试验的入组人群(平均约45岁)比OASIS系列(平均48-50岁)略为年轻。在性别分布上,OASIS系列体现了典型的肥胖临床试验特征,女性占比极高(73% - 85%左右);而ATTAIN-1为了保证男性样本的充足,人为设定了女性入组上限(70%上限),最终使其女性比例控制在64%左右。已知在基于肠促胰岛素的减重疗法中,男性的体重下降幅度通常低于女性,这一性别分布的差异可能导致ATTAIN-1 的整体减重数据在跨试验对比时受到轻微的不利影响 。 -
种族多样性与全球化代表性: OASIS-4 试验呈现出压倒性的白人主导特征(白人占比高达约90%),亚裔仅占不足1%。相反,ATTAIN-1试验展现了极强的全球化招募能力,不仅总样本量庞大(>3000人),且亚裔人口占比高达约29%,白人占比降至55%左右。种族的巨大差异可能导致代谢基因型和身体体成分分布的不同,从而对药物的代谢清除率和脂肪重新分布产生影响。
有效性对比洞察
-
在OASIS-1试验中,极高剂量(50 mg)口服司美格鲁肽展现了统治级的减重压制力。在第68周,患者平均体重较基线骤降-15.1%,扣除安慰剂效应(-2.4%)后,净估计治疗差异高达-12.7%。这一成绩不仅彻底刷新了口服减重药物的疗效天花板,甚至已经逼近甚至部分重叠了其皮下注射版本Wegovy(2.4 mg每周一次,在STEP-1试验中平均减重约14.9%)的疗效下限,证明了只要突破了肠道吸收屏障并给予足够的剂量补偿,多肽分子的全身性受体激活能力依然无可匹敌。
-
在OASIS-4试验中,标准剂量(25 mg)口服司美格鲁肽在第64周同样交出了优异的平均减重-13.6%,净估计治疗差异为-11.4%。值得注意的是,剂量减半(从50 mg降至25 mg)并未导致疗效的线性折半,仅牺牲了约1.5%的绝对减重效果。这表明口服司美格鲁肽在25 mg左右的剂量区间可能已经接近了大多数患者胃肠道受体敏感性与中枢神经饱和度的效能拐点,更高的剂量更多是在弥补个体间吸收变异率,而非无限制地提升受体激活的绝对上限。
-
在ATTAIN-1试验中,作为小分子代表的Orforglipron在经历了漫长的滴定期后,在第72周的疗效节点上,其最高剂量(36 mg)组实现了-11.2%的平均体重下降,净估计治疗差异为-9.1%。其较低的12 mg和6 mg剂量组分别实现了-8.4%和-7.5%的减重 。
结论:在考量现实世界效益时,11.2%(Orforglipron 36mg)对比13.6%(Oral Sema 25mg)与15.1%(Oral Sema 50mg)的阶梯式落差,客观上暴露出第一代小分子非肽类激动剂在受体空间构象的结合效率或透过血脑屏障深入下丘脑食欲调节中枢的能力上,可能仍略逊于经过自然进化与生化修饰双重复调的结构修饰多肽。
有效性的其他考量
减重并非单纯的脂肪消除,其最终的医学诉求是打破由内脏脂肪堆积引发的系统性代谢紊乱。在这一维度上,GLP-1受体激动剂展现出了超越单纯体重减轻的多效性靶器官保护作用。
-
血压与体脂分布: 在ATTAIN-1、OASIS-1和OASIS-4中,两款药物均促使患者的收缩压(SBP)和腰围实现了具有临床统计学意义的显著降低。腰围的显著缩小直接对应着内脏异位脂肪的消除。
-
脂质代谢网络: 脂质毒性是动脉粥样硬化性心血管疾病(ASCVD)的加速器。ATTAIN-1的详细数据证实,Orforglipron不仅有效降低了甘油三酯(TG)水平,更显著降低了非高密度脂蛋白(Non-HDL)胆固醇水平。Non-HDL胆固醇是包含了所有致动脉粥样硬化脂蛋白(包括LDL、VLDL等)的综合指标,其下降直接预示着血管内皮脂质沉积风险的降低。
-
身体机能与生活质量的回归: 在OASIS-4试验中,研究者采用了针对肥胖症设计的IWQOL-Lite-CT量表进行评估。结果显示,口服司美格鲁肽25 mg组患者的身体机能得分较安慰剂组获得了极具统计学意义的提升(P<0.001),高达55.3%的用药组患者实现了至少14.6分的具有临床意义的身体机能改善(安慰剂组仅为34.8%)。这意味着由于重度肥胖导致的关节承重过载、活动气促和日常行动受限得到了实质性的解除。
综上,无论是多肽类的口服司美格鲁肽还是小分子的Orforglipron,均能将体重的减轻成功转化为下游的心脏代谢获益与生活质量的提升,进一步巩固了GLP-1受体激动剂作为肥胖多系统并发症基础疗法的地位。
安全性对比洞察
在OASIS-1(50 mg口服司美格鲁肽)中,整体不良事件(AE)发生率为92%,其中胃肠道不良事件高达80%。在OASIS-4(25 mg口服司美格鲁肽)中,胃肠道不良事件发生率略降至74.0%。值得高度关注的是,尽管遭遇了如此高频的胃肠道反应,但试验明确指出这些症状“绝大多数为轻度至中度且呈一过性”,并未导致灾难性的停药。患者的消化系统在经历了初期的药物应激后,展现出了良好的耐受性适应能力。
将目光转向ATTAIN-1。作为一款小分子药物,Orforglipron在剂量递增期(1 mg至36 mg,历时近5个月)采用了极为谨慎的滴定策略,意在通过延长适应期来缓解中枢化学感受器触发区的呕吐反射。最终结果显示,各剂量组(6 mg、12 mg、36 mg)的总体不良事件发生率在83.4%至86.6%之间。然而,在最核心的因不良事件导致治疗中止(停药率)这一硬指标上,Orforglipron暴露出其软肋:因不良事件停药的比例高达5.3%至10.3%(36 mg高剂量组通常对应最高停药率),而安慰剂组仅为2.7%。而在单独评估因胃肠道不良事件(GI AEs)导致的停药率时,Orforglipron在各个维度的停药数据均不容乐观。
此外,在ATTAIN-1试验当中,一个不容忽视的安全信号被记录在案:报告了5例经由独立裁定委员会确认的轻度胰腺炎病例,均发生于Orforglipron治疗组,且其中一例因影像学检查确认为梗阻性胰腺炎。虽然没有严重并发症的报告,且多数仅基于症状和生化酶水平升高,有潜在的风险。同时,Orforglipron组还观察到平均心率每分钟上升4.3至5.3次的现象,这与肽类GLP-1的已知生理效应相一致,但仍需在更长期的心血管终点试验中予以密切监控。
总结
综合ATTAIN-1、OASIS系列临床,我们可以得出结论:口服司美格鲁肽 与 Orforglipron并非只在减重领域厮杀,而是对整个代谢疾病的控制都展现出治疗潜力,从多方面大幅提升肥胖人群的获益。
从分子药理效能和靶器官耐受的绝对统治力来看,二者有一定的互补性。
-
基于SNAC技术的口服司美格鲁肽在50 mg及25 mg的剂量下,展示了多肽类药物在疗效和胃肠道长期耐受性平衡上的标杆地位。其-15.1%的深层减重突破、超过三分之一患者达成的20%以上“类手术”级体重缩减,以及经受住人群检验的较低不良事件停药率,使其成为追求极致减重效果、对副作用极度敏感,且个人自律性极强、能够严格遵守晨间空腹给药程序的精英患者群体及临床专家的首选武器。 -
礼来的小分子 Orforglipron 代表了一个属于未来的范式。虽然在绝对疗效和早期胃肠道阵痛为代价,换取了颠覆性的临床便利性——无论何时、无论饥饱的随时给药自由。更具决定意义的是,小分子化学合成工艺所赋予的极低制造成本和无限供给弹性,使其具备了将昂贵的GLP-1疗法从发达国家的“精英特权药”降维普及为全球中低收入地区、基层初级保健系统以及海量下沉医保市场的“大众普适药”的革命性潜能。
在可预见的未来十年,随着口服GLP-1药物市场的全速爆发,这两条不同分子路径的战略互补将共同把代谢疾病治疗体系推向史无前例的广度。