
近日,《Nature Reviews Cancer》近期发表了一篇深度综述,全面剖析了“情境依赖性合成致死”(Context-dependent synthetic lethality)这一领域的前沿进展、底层机制以及未来的转化方向。今天,对这篇重磅文献进行总结。
一、 什么是“合成致死”?
合成致死的概念非常巧妙:它利用了癌细胞因特定基因或细胞状态改变而产生的独特功能脆弱性,而这些脆弱性在正常细胞中是不存在的。简单来说,当只有条件A或条件B单发时,细胞安然无恙;但当A和B同时失去功能时,细胞就会走向死亡。
这种策略的强大之处在于,它能精准打击癌细胞,而放过健康组织。那么,哪些“遗传背景”会触发这种致命的弱点呢?综述总结了四大类:
-
直接的致癌基因激活:致癌通路的激活不仅会驱动肿瘤生长,还会让癌细胞对该通路产生“成瘾性”。例如,BRAF突变的癌细胞会对下游的MEK和ERK节点产生高度依赖,从而创造了合成致死机会。
-
抑癌基因缺失:这是目前临床最成功的领域。最著名的例子就是BRCA1和BRCA2基因突变导致同源重组修复缺陷(HRD),使得这类癌细胞必须依赖PARP酶来生存。PARP抑制剂正是利用了这一合成致死关系,在临床上取得了巨大成功。
-
“搭车”缺失(Passenger deletions):在肿瘤进化过程中,某些关键的抑癌基因被删除时,附近的基因也会跟着“倒霉”。例如,肿瘤抑制基因CDKN2A的缺失往往伴随着邻近MTAP基因的丢失。这种缺失为靶向PRMT5或MAT2A创造了绝佳的合成致死窗口。
-
基因组不稳定性:例如微卫星不稳定(MSI-H)肿瘤因DNA错配修复缺陷,会形成异常的十字形DNA结构,这使得它们极度依赖WRN解旋酶来解开这些结构。抑制WRN会导致癌细胞DNA碎裂死亡。
二、合成致死的底层核心机制
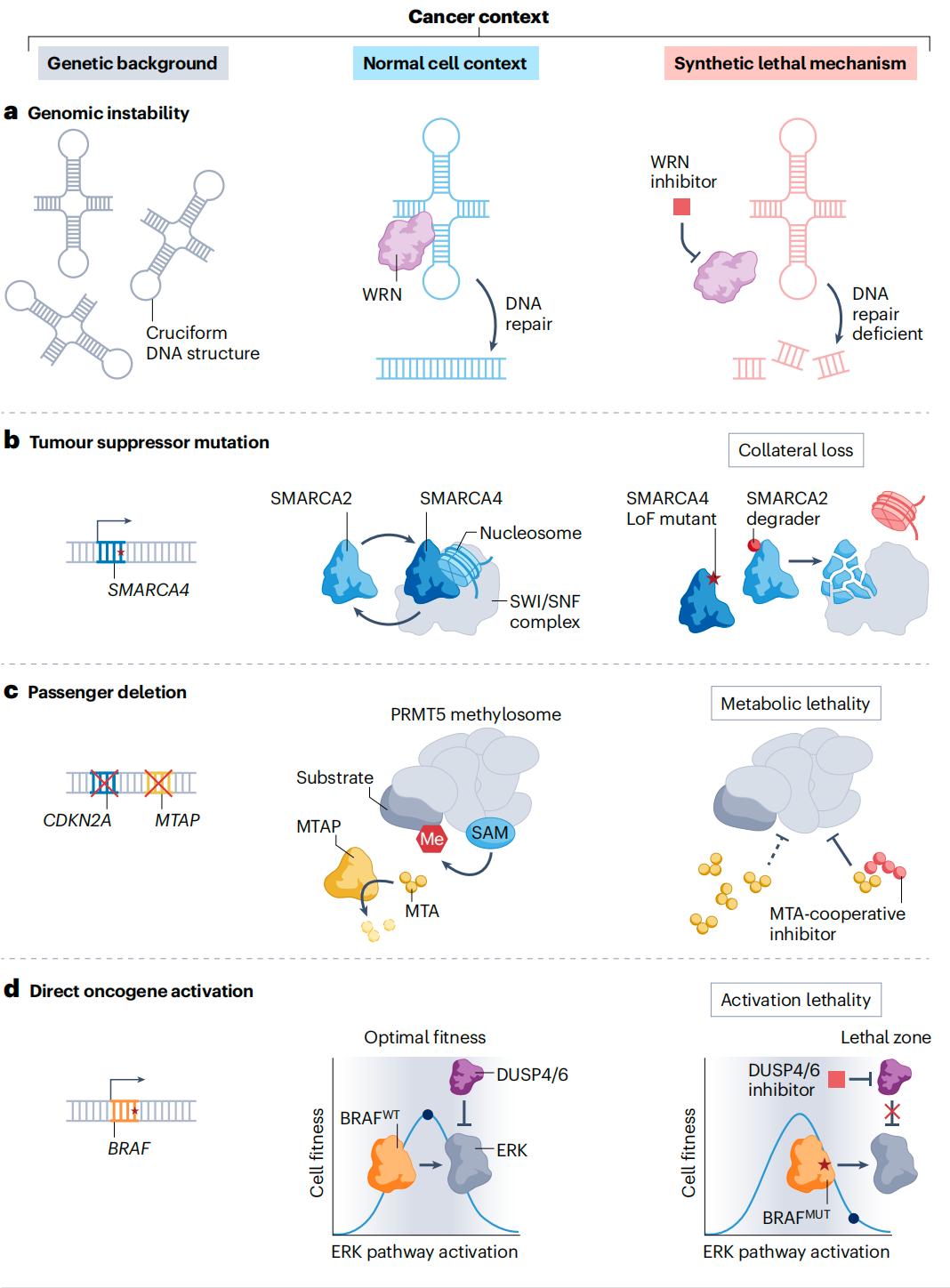
深入理解分子机制是指导药物设计的关键 。研究揭示了合成致死背后的几种常见运作模式:
-
DNA修复缺陷:正如上文提到的PARP和WRN,许多癌症存在背景性的DNA修复途径变异,导致它们必须依赖替代性的修复途径来存活。 -
冗余必需基因的“旁系同源”丢失:正常细胞通常有互为“备胎”的旁系同源基因。当癌细胞丢失了其中一个(例如SWI/SNF复合物中的SMARCA4),另一个(SMARCA2)就会变成其生存的唯一依赖。此时降解SMARCA2,就能精准杀死癌细胞。 -
代谢致死:由于MTAP缺失,代谢物MTA会在癌细胞中大量积累。MTA会与PRMT5酶结合并部分抑制其活性,从而导致MTAP缺失的细胞对PRMT5抑制剂异常敏感。 -
通路过度激活致死(Activation lethality):合成致死不一定非要“抑制”。研究发现,在具有BRAF或NRAS突变的肿瘤中,如果抑制其负反馈调节因子(如DUSP4和DUSP6),会导致ERK信号通路过度激活,这种“信号过载”反而能毒死癌细胞。
三、主流合成致死靶点与临床研发Landscape
为了让大家更直观地了解目前的研发格局,我们提炼了综述中极具代表性的合成致死靶点及其最新临床状态。从中我们可以看到,除了已经大获成功的PARP抑制剂,针对PRMT5、WRN、CDK2等靶点的药物正处于火热的临床阶段。
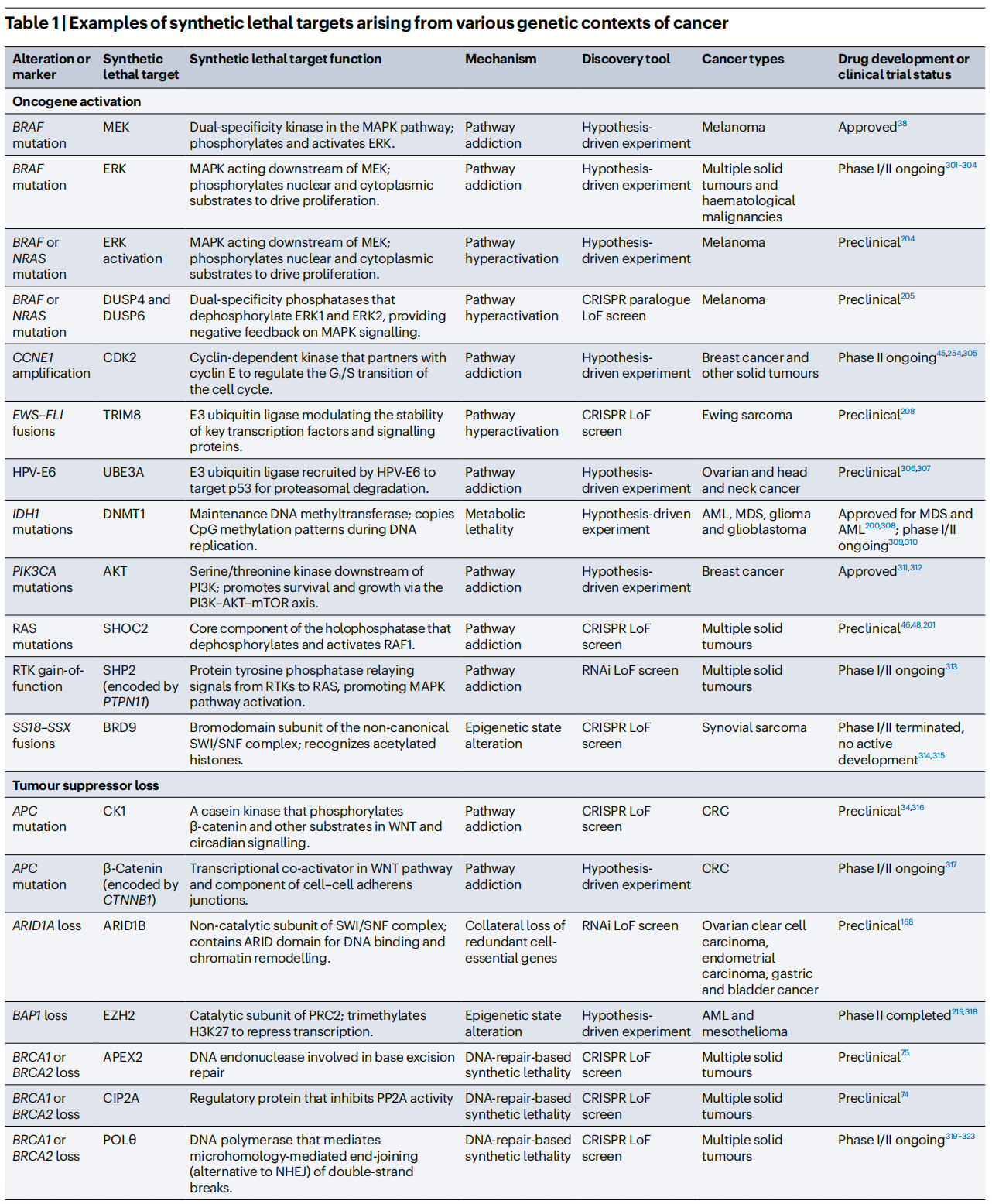
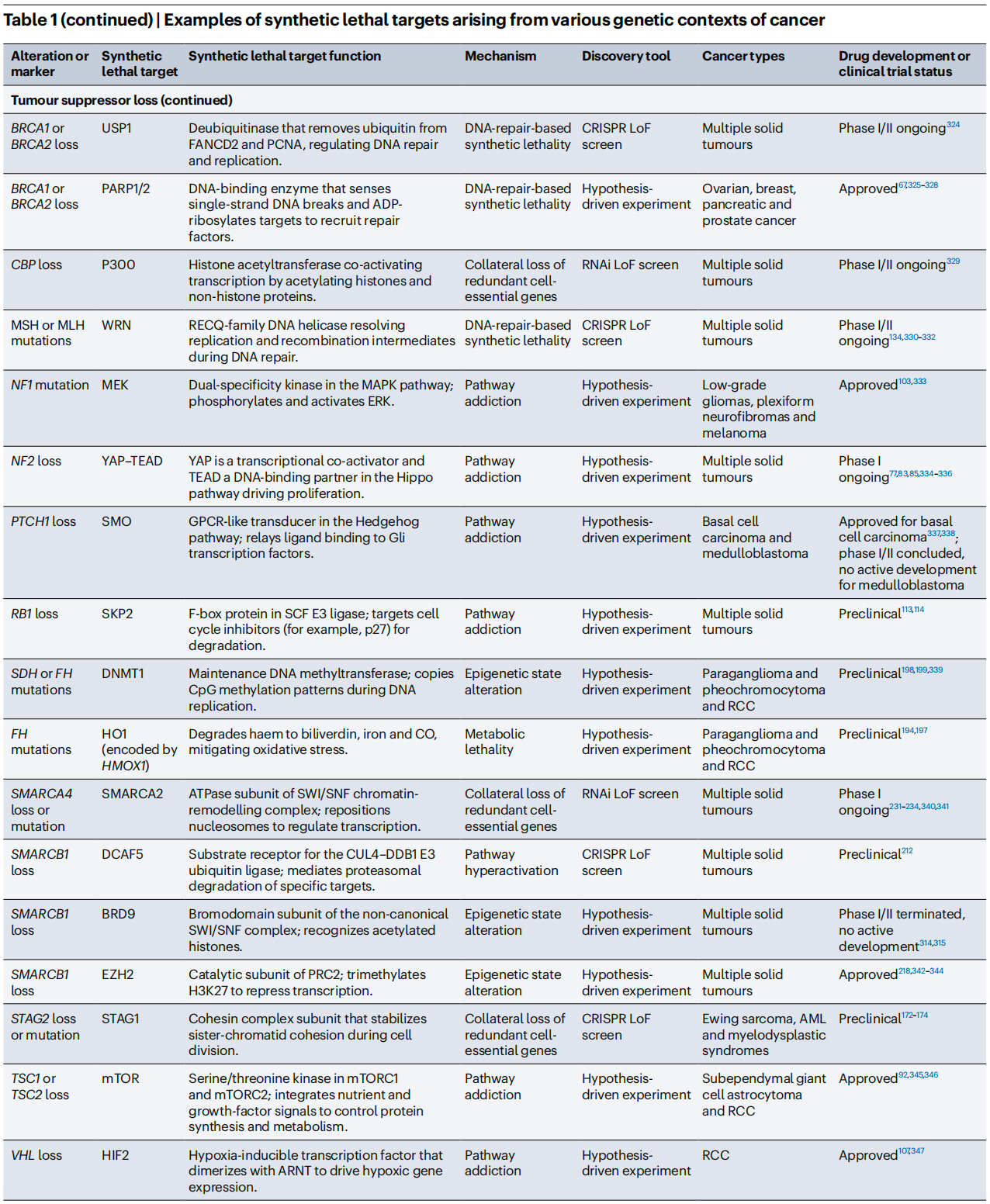
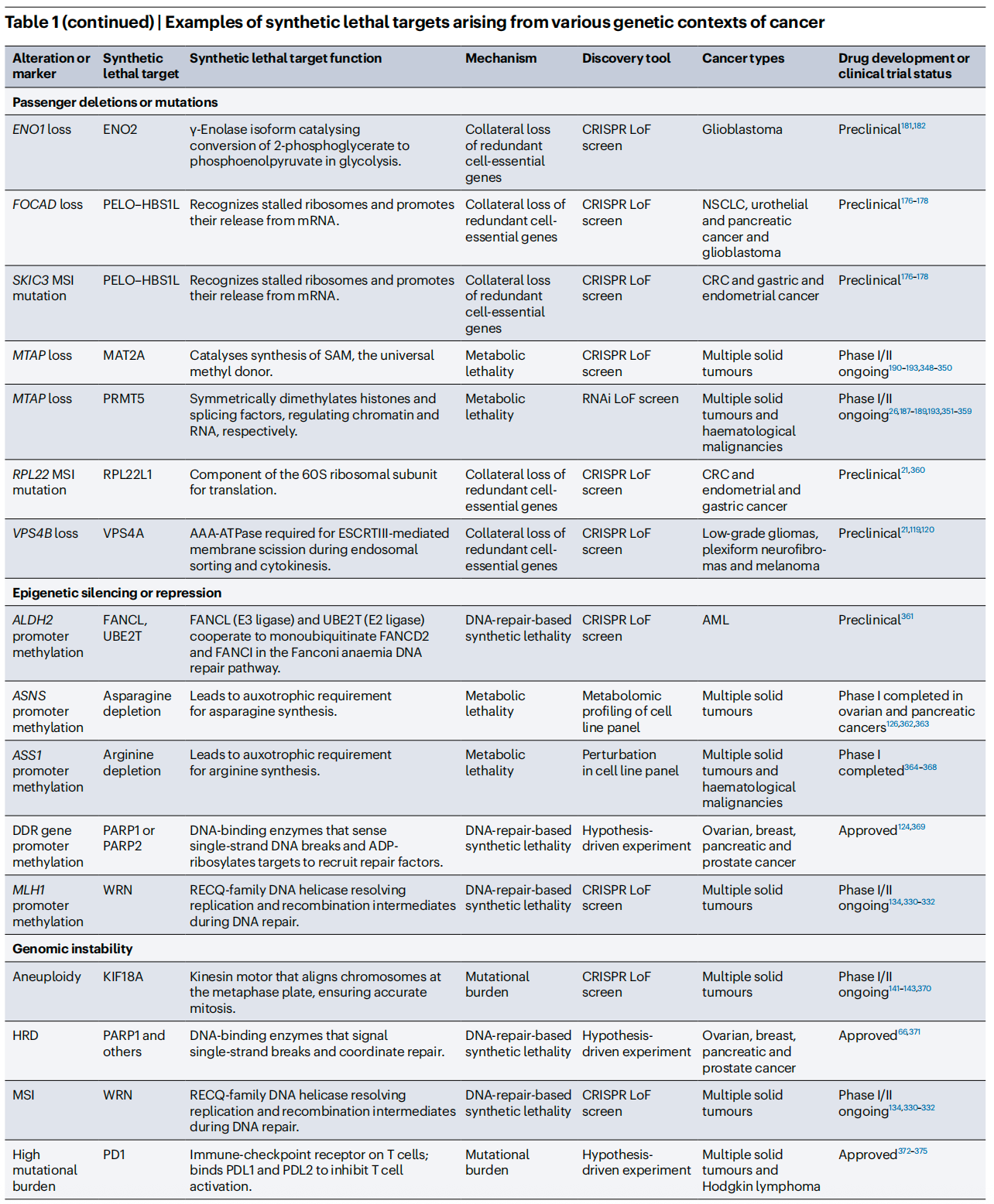

四、从实验室到临床
尽管PARP抑制剂在前,但并非所有合成致死靶点都能顺利成药。这篇综述指出了临床转化必须关注的两大核心:
治疗指数(Therapeutic Index)是成败的关键:靶点的安全性存在明显的“梯度”。像PARP和WRN这样的靶点,其脆弱性高度集中在特定生物标志物阳性的癌细胞中,治疗指数宽泛,安全性高。相反,像WEE1或ATR这样的靶点,在多细胞系中表现出广泛的致死性(泛必需基因),导致其临床试验中常出现严重的血液和胃肠道毒性,限制了用药。
治疗机制不仅限于基因敲除:CRISPR筛选出的“基因丢失”不等于现实中的“酶活性抑制” 。例如针对SMARCA4突变的癌症,传统的非选择性抑制剂无法区分正常细胞和癌细胞,而开发特异性的蛋白降解剂(PROTAC)似乎才是实现选择性杀伤的正确路径。
五、挖掘下一代“神药”靶点
传统的单基因敲除筛选已经趋于饱和,为了寻找新的突破口,未来的发现策略必须升级 :
-
多基因联合筛选:通过组合CRISPR技术,挖掘那些在单基因扰动中被隐藏的双重依赖关系(如DUSP4/DUSP6)。 -
蛋白质层面的单碱基编辑筛选:超越简单的基因敲除,在单个氨基酸的精度上寻找蛋白质结构域的脆弱点。 -
AI与机器学习的介入:面对涵盖上千种癌细胞系和海量多组学数据(如DepMap项目),利用人工智能模型可以挖掘出人类统计学方法难以察觉的全新合成致死基因对。
六、结论
合成致死策略正在将肿瘤精准治疗推向一个更深、更广的新维度。通过将遗传背景与精细的分子机制相融合,并结合新型药物形式(如降解剂和别构抑制剂),未来会有更多具备优异疗效和安全性的合成致死抗癌药物走出实验室。