
2026年4月23日,FDA 加速批准再生元(Regeneron)的创新基因疗法 Otarmeni(lunsotogene parvec-cwha) 上市。这是全球首款用于治疗遗传性耳聋的AAV载体基因疗法,从提交BLA申请到获批仅用了短短61天!
再生元宣布,将在美国免费提供这款具有划时代意义的突破性药物。
OTOF基因与“无声世界”
听力损失是全球最常见的感官缺陷之一,而在先天性耳聋中,约有一半是由基因突变引起的。Otarmeni此次获批的适应症,专门针对由 OTOF(Otoferlin,耳铁蛋白)基因双等位基因致病变异 引起的重度至极重度感音神经性耳聋(任何频率>90 dB HL)的儿童和成人患者。
OTOF基因负责编码耳铁蛋白(Otoferlin),这是一种在内耳毛细胞中起关键作用的蛋白质,负责将声音信号转化为神经冲动并传递给听觉神经。一旦该基因发生突变,患者虽然耳部物理结构完整,但大脑却根本无法接收到内耳传来的声音信号。
这是一种极其罕见的疾病,在美国每年约有20到50名新生儿受此影响。过去,对于这类OTOF相关的遗传性耳聋,医学界没有任何可以改变疾病进程的药物。患者唯一的选择是植入人工耳蜗,但这终究无法完全还原自然的听力感受。由于疾病导致的听觉剥夺,许多患儿错过了语言发育的黄金窗口期,面临终身的言语和认知发育迟缓。
临床数据:一次注射,重获自然听力
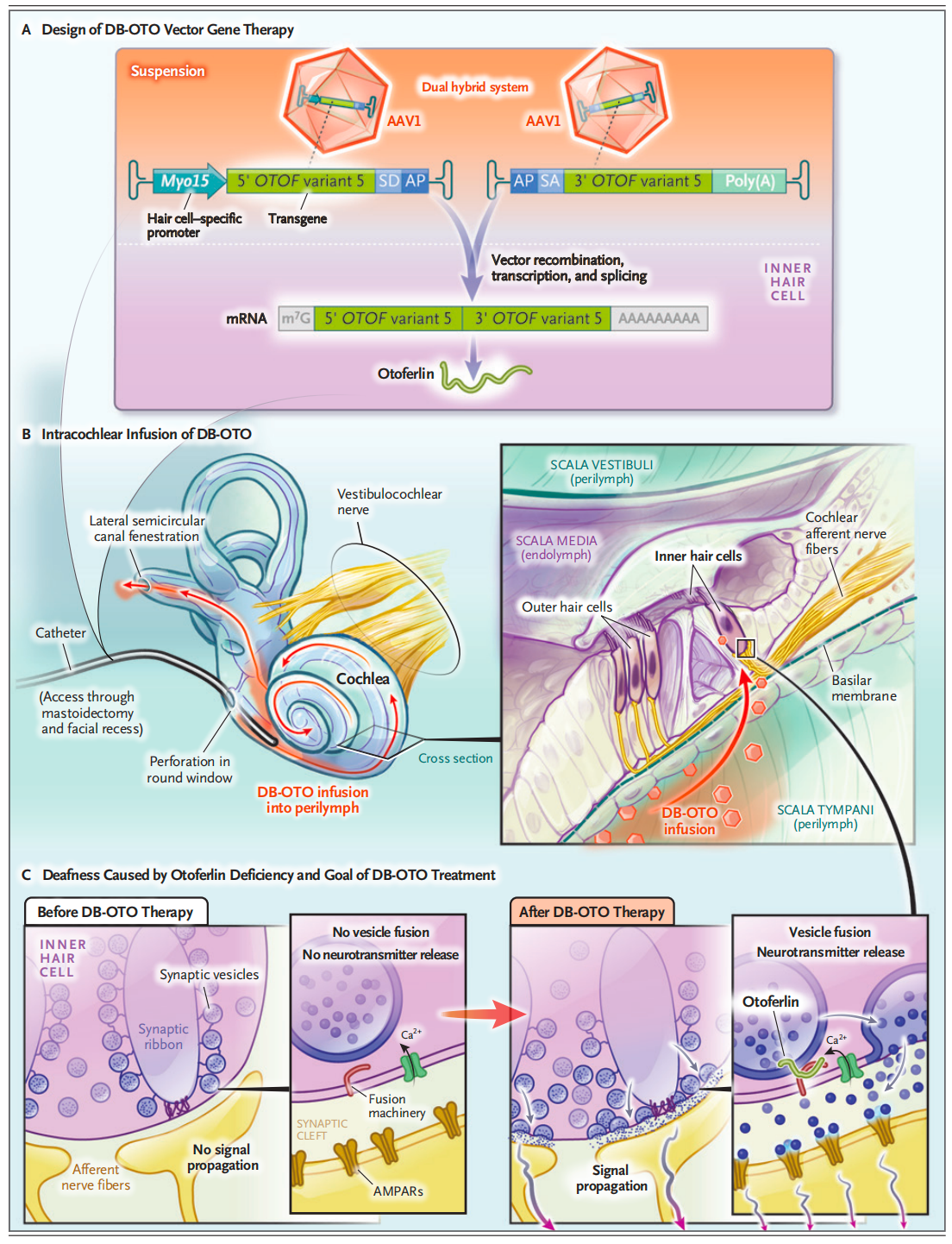
(图片来自NEJM)
Otarmeni 作为一款基于双腺相关病毒(AAV1)载体的基因疗法,Otarmeni通过一次性的微创手术(在全身麻醉下,采用类似人工耳蜗植入手术的途径进行内耳注射),将功能正常的OTOF基因精准递送至内耳的毛细胞中,从而原位恢复耳铁蛋白的产生和听觉信号的传导。
临床数据近期已在《新英格兰医学杂志》上发表。在名为CHORD的Phase 1/2期单臂临床试验中,研究人员评估了24名年龄在10个月至16岁之间的儿童患者。
-
在20名可评估疗效的患者中,高达80%(16名)的患者在治疗24周内听力得到了显著改善,达到了≤70 dB HL的纯音测听(PTA)阈值(即不再必须依赖人工耳蜗的临床标准)。
-
随着随访时间的延长,42%的患者听力直接恢复到了正常范围,甚至能够清晰地听到耳语!
-
除了听力阈值的改善,患儿在言语感知和语言发育上也取得了重大突破。在没有视觉提示的情况下,部分患儿能够准确识别双音节词汇(如“妈妈”、“饼干”),并在嘈杂环境中对远处的言语做出反应。这意味着,他们真正实现了全天候(24/7)自然听力的恢复。
“光速”审批
该药物是FDA“专员国家优先审查凭证(CNPV)”试点项目下批准的第六款产品,也是该项目下诞生的首款基因疗法。凭借其突破性的疗效数据和解决未满足医疗需求的巨大潜力,Otarmeni在提交BLA后仅仅61天便获得了加速批准。
FDA局长Marty Makary医学博士对此高度评价:“今天的批准是遗传性耳聋治疗的一个重要里程碑。通过CNPV试点项目,FDA证明了我们完全有能力在极短时间内,成功且高效地审查诸如新型双载体基因疗法这样极其复杂的申请,加速将救命疗法带给有需要的罕见病患者。”
全美免费提供
基因疗法向来以研发成本高昂和“天价”账单著称(动辄数百万美元),但再生元制药在此次产品上市时却做出了一个震撼医药界和社会的决定。作为与美国政府达成降低美国患者药品成本协议的一部分,再生元宣布将在美国范围内完全免费提供Otarmeni。
再生元董事会联合主席、总裁兼首席科学官 George Yancopoulos 博士在一份声明中深情地表示:“Otarmeni是一次巨大的科学飞跃,也是对‘当聪明的大脑拥有资源和自由去挑战难题时能创造何种奇迹’的有力证明。当我们看到CHORD试验中那些令人惊叹的数据时,我们讨论的是如何确保这项科学突破能够帮助尽可能多的人。我们决定在美国免费提供Otarmeni,这突显了我们的坚定信念——生物制药行业可以、也应该成为世界上真正的向善力量。”