2025年10月8日,恒瑞医药在clinicaltrials.gov公开启动针对SHR-1905治疗中度至重度特应性皮炎的2期临床(NCT07211542),预计招募20为名患者,研究预计2025年11月正式启动。
SHR-1905是恒瑞自主研发的新型长效抗胸腺基质淋巴细胞生成素(TSLP)单克隆抗体。2025年8月,恒瑞连续公开启动SHR-1905针对重度哮喘临床3期(NCT07098403)和慢性伴鼻息肉的慢性鼻窦炎临床2期(NCT07132827)试验,同步推进自勉三项适应症,标志着恒瑞医药在拓展其关键自免疫管线上的决心。
SHR-1905的关键临床
SHR-1905是一种人源化的免疫球蛋白G1(IgG1)kappa型单克隆抗体,其设计旨在特异性结合并抑制TSLP的生物活性 。通过阻断TSLP这一上游炎症信号,SHR-1905旨在中断下游多种炎症细胞因子的释放,从而控制多种过敏性和自身免疫性疾病的核心炎症级联反应。
关键的1期临床NCT04800263:80天超长半衰期
安全性与耐受性: 在50-600 mg的剂量范围内,该药物展现出良好的安全性。大多数治疗期间出现的不良事件(TEAEs)为轻度,其发生率与安慰剂组相当。
免疫原性: 仅有15%的受试者检测到抗药抗体(ADAs),且这些抗体的出现并未对药物的药代动力学(PK)或安全性产生明显影响,表明其免疫原性风险较低。
药代动力学 (PK): PK数据显示出两个核心特征:药物暴露量呈略高于剂量比例的方式增加;以及最为关键的一点,其血清半衰期被证实长达约80天。
SHR-1905在I期临床中展现的约80天超长半衰期,这为其实现每6个月给药一次的方案提供了可能 。当前TSLP抑制剂市场的领导者Tezspire(Tezepelumab,特泽鲁单抗,阿斯利康研发)的给药频率为每四周一次皮下注射,这已成为该领域的便利性基准。
从每年13次注射(Tezspire)锐减至可能每年仅需2次注射(SHR-1905),这并非简单的增量改进,而是对治疗模式的颠覆性变革。对于需要长期管理的慢性疾病(如哮喘和特应性皮炎)患者而言,这种治疗负担的显著降低,将极大地提升生活质量和长期用药依从性,构成极具吸引力的产品优势。
重磅交易
2023年8月,恒瑞医药达成了一项重大的战略合作,将SHR-1905在大中华区以外的全球开发、生产及商业化独家权利授予One Bio公司(后改名Aiolos Bio,2024年被GSK收购)。协议包括2150万美元的首付款,以及高达10.25亿美元的潜在开发和销售里程碑付款,外加基于年净销售额的分级、达到两位数的销售提成。
TSLP竞争格局
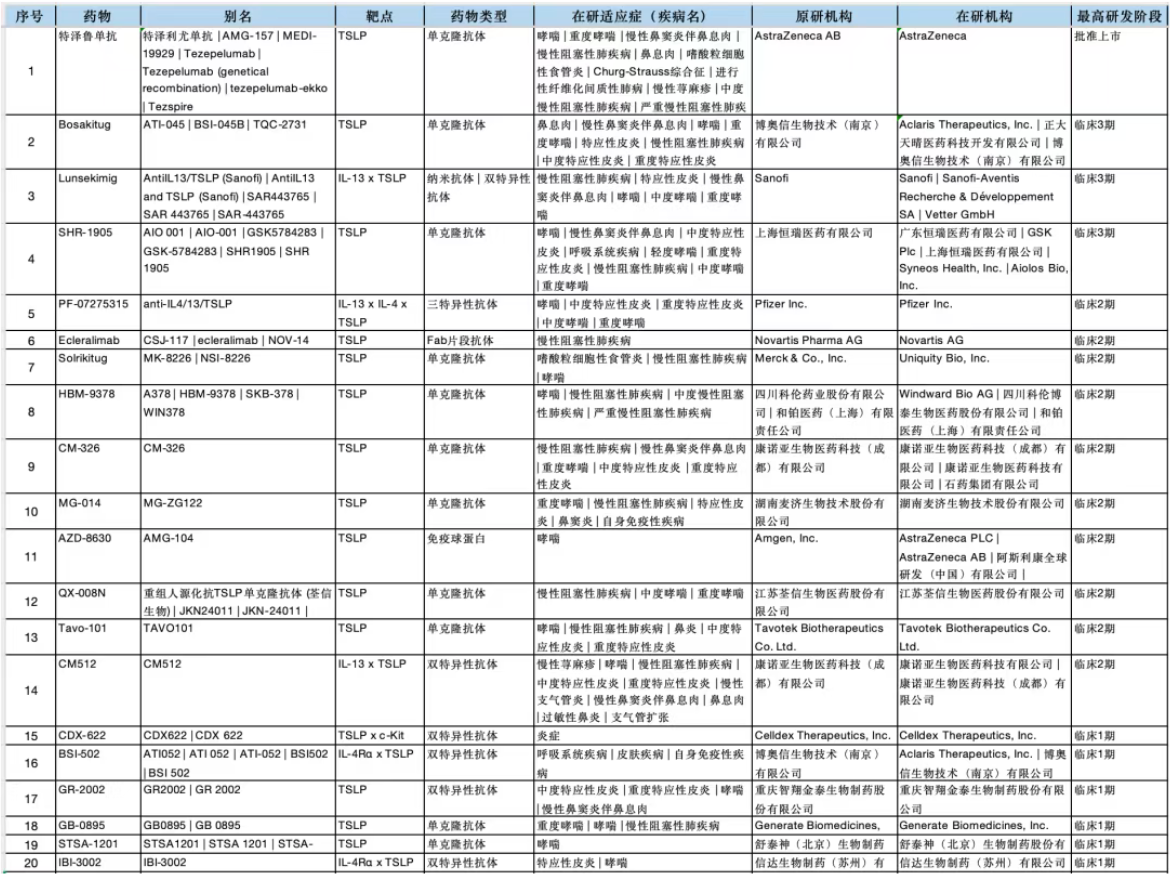
根据智慧芽新药情报数据库,目前全球TSLP抑制剂管线包括68个,下面列出top20管线。
Reference:
1. https://clinicaltrials.gov/study/NCT07211542
2. https://firstwordpharma.com/story/5770458
3. https://pubmed.ncbi.nlm.nih.gov/39076593/