一、摘要
在当今全球新药研发中,细胞免疫疗法正经历着从血液瘤向实体瘤跨越的关键转折期。作为过继性细胞疗法的重要分支,肿瘤浸润淋巴细胞疗法(下文简称TIL疗法)因其天然的肿瘤识别能力和多靶点特异性,被视为攻克实体瘤的希望。本报告旨在对TIL疗法进行详尽的调研与分析,剖析其在药企立项、商务拓展(BD)中的战略价值。
2024年2月,美国FDA批准Iovance Biotherapeutics的Lifileucel(商品名:Amtagvi)上市,用于治疗晚期黑色素瘤,这标志着全球首款针对实体瘤的T细胞疗法正式进入商业化阶段。这一里程碑事件不仅打破了CAR-T疗法局限于血液瘤的局限,更验证了TIL疗法的可行性,极大地提振了行业信心。然而,TIL疗法领域正处于剧烈的洗牌与分化期。
本报告将深入剖析TIL疗法的技术演进逻辑,梳理全球及中国市场的竞争格局,详解关键的BD交易案例,并对未来的技术发展趋势做出前瞻性研判,为制药企业的战略决策提供坚实的情报支撑。
二、TIL疗法技术的背景
2.1 技术原理与作用机制
TIL疗法的核心理念在于“取之于瘤,用之于瘤”。其生物学基础源于对肿瘤微环境(Tumor Microenvironment, TME),在肿瘤组织内部,天然存在着一群淋巴细胞(主要是T细胞),它们已经识别了肿瘤抗原并迁移至肿瘤部位,试图对癌细胞进行杀伤。然而,在进展期癌症患者体内,这群“先遣部队”往往处于劣势——它们的数量不足以压倒肿瘤的生长速度,或者被肿瘤微环境中的免疫抑制信号(如PD-L1、TGF-β)所“耗竭”或“驯化”,从而丧失了杀伤功能。
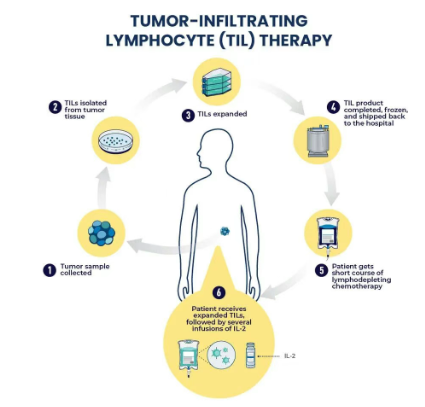
(图片来自NIH)
TIL疗法的制备与治疗流程是一个复杂的自体细胞工程:
1)肿瘤切除与取材:通过外科手术切除患者的肿瘤组织(通常需要直径1.5cm以上),并在GMP实验室中将其处理成微小的肿瘤碎片或单细胞悬液。
2)体外分离与复苏:将肿瘤碎片置于含有高浓度白介素-2(IL-2)的培养基中。IL-2作为T细胞生长因子,能够使得T细胞从肿瘤基质中迁出并开始增殖,同时逆转其在体内的耗竭状态,恢复其杀伤活性。
3)快速扩增(REP):当TIL细胞扩增到一定数量(如几千万个)后,启动快速扩增程序(Rapid Expansion Protocol)。利用抗CD3抗体、高剂量IL-2以及经辐照处理的饲养细胞(通常为异体外周血单个核细胞),在14天左右将T细胞数量扩增至数十亿甚至上百亿级别(10^9 - 10^11)。
4)清淋预处理:在回输TIL之前,患者需接受非清髓性的化疗方案(通常是环磷酰胺+氟达拉滨),即“清淋”。这一步至关重要,其目的是清除患者体内的抑制性免疫细胞(如Treg细胞),消除对细胞因子的竞争,从而为回输的TIL细胞创造一个更有利于定植和扩增的体内环境。
5)回输与支持治疗:将制备好的TIL细胞一次性回输给患者,随后给予多次高剂量的IL-2注射,以支持TIL在体内的持续存活与抗肿瘤活性。
2.2 适应症布局
由于TIL细胞源自肿瘤组织,其天然具备识别肿瘤特异性抗原的能力,因此在实体瘤治疗中展现出广阔的潜力。
1)黑色素瘤:这是TIL疗法的“大本营”。黑色素瘤具有极高的肿瘤突变负荷(TMB),产生了大量的新抗原,使得TIL极其丰富且特异性强。Lifileucel的获批正是基于其在PD-1抗体治疗失败后的晚期黑色素瘤患者中取得的优异数据。
2)非小细胞肺癌:作为全球发病率最高的癌症之一,NSCLC也是TIL疗法重点攻克的领域。吸烟导致的基因突变同样能产生丰富的新抗原。Iovance的LN-145管线在此领域已取得突破性数据。
3)宫颈癌:HPV病毒感染驱动的宫颈癌表达病毒抗原(E6/E7蛋白),这为TIL提供了明确的非自身靶点,使其成为TIL疗法响应率较高的癌种之一。
4)其他实体瘤:头颈部鳞状细胞癌(HNSCC)、三阴性乳腺癌、结直肠癌、肝癌等也在积极探索中,尽管在低突变负荷的“冷肿瘤”中,传统TIL疗法面临更大挑战。
2.3 技术优势与竞争壁垒
相较于现有的免疫检查点抑制剂(如PD-1等)和其他细胞疗法(CAR-T, TCR-T等),TIL疗法具有独特的技术优势,同时也构建了较高的行业壁垒。
1)多靶点多克隆性:这是TIL与CAR-T/TCR-T最本质的区别。CAR-T通常只针对单一表面抗原(如CD19),容易因抗原丢失而复发;TCR-T针对特定的单一抗原肽-MHC复合物。而TIL包含成百上千种不同的T细胞克隆,能够同时识别肿瘤的多种新抗原。这种“集团军作战”模式使得肿瘤很难通过下调某单一抗原而逃逸,极大地降低了耐药风险。
2)天然的肿瘤归巢能力:TIL细胞本身就取自肿瘤微环境,它们天然表达能够趋化至肿瘤部位的受体。相比于外周血来源的CAR-T细胞,TIL在回输后能更高效地穿透实体瘤的基质屏障,浸润到肿瘤内部。
3)安全性相对可控:由于TIL识别的是肿瘤新抗原(仅在肿瘤细胞表达),而非正常组织抗原,因此发生“脱靶效应”的风险显著低于基因工程改造的TCR-T疗法。
4)CMC工艺的极端复杂性:TIL的起始物料是患者的肿瘤组织,其质量、大小、活性因人而异。如何从坏死组织多、肿瘤细胞少的样本中稳定扩增出数十亿计的高活性T细胞,是核心的工艺壁垒。Instil Bio的失败正是因为无法保证生产成功率。
5)供应链与物流挑战:这就要求药企必须建立极高标准的冷链物流体系和中央实验室处理能力。Iovance花费数年时间,通过建立费城生产基地(iCTC)并验证冷冻保存技术,才实现了商业化的可能,将原本必须“鲜活回输”的限制打破,使得全球发货成为可能。
三、竞争格局
全球TIL疗法领域呈现出“一超多强、分化加剧”的局面。以Iovance为首的第一梯队已跨过商业化门槛,而以Obsidian、KSQ为代表的第二梯队正通过基因改造技术试图实现“弯道超车”。与此同时,中国企业凭借在工艺上的快速迭代和临床资源的优势,正在成为不可忽视的重要力量。
目前全球TIL疗法总共137条管线,由于篇幅有限,下面列出的处于临床一期以上的管线总共54条(读者可以加文末助理微信获取完整竞争格局)。
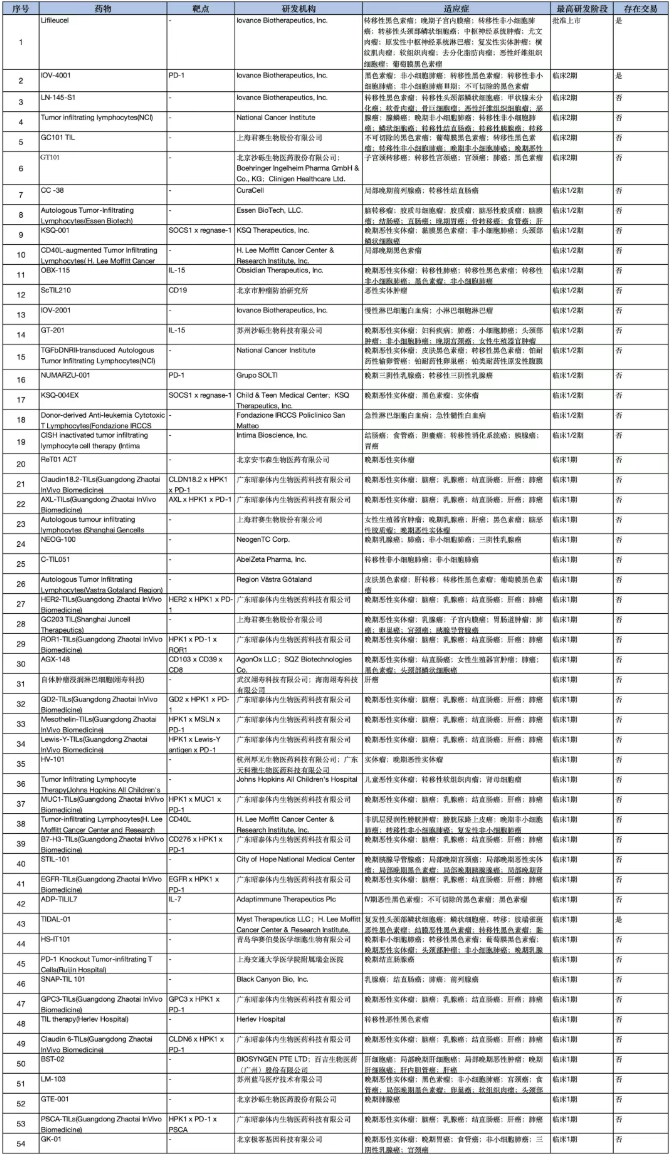
全球竞争格局头部企业
1. 商业化领跑者 Iovance Biotherapeutics
核心管线:Lifileucel (Amtagvi),已获批上市(2024年2月,FDA加速批准)。适应症:既往接受过PD-1抗体治疗(若为BRAF突变阳性则需接受过BRAF抑制剂治疗)的不可切除或转移性黑色素瘤。
关键临床数据:在关键性2期临床试验中,Lifileucel展现了令人瞩目的疗效。在多线治疗失败(平均既往接受过3.3种治疗)的晚期黑色素瘤患者中,客观缓解率 ORR 达到 31.5%。更重要的是响应的持久性。中位缓解持续时间 mDOR 在数据截止时仍未达到,意味着许多患者在单次输注后实现了长达数年的无癌生存。这在晚期实体瘤治疗中是极具颠覆性的。
安全性与局限:Amtagvi的标签中包含关于治疗相关死亡、严重血细胞减少、严重感染以及心肺肾功能损害的黑框警告。这主要归因于清淋化疗和高剂量IL-2的使用,限制了其只能在具备ICU支持的中心开展。
目前Iovance的开发策略是围绕Lifileucel进行适应症拓展和联合疗法,同时推进后续管线开展。

2. 沙砾生物 (GRIT Biotechnology)
核心管线:GT101,第一代未经基因修饰的TIL产品,是中国首个获批IND的TIL疗法。目前处于2期临床阶段,计划2025年提交NDA。其在晚期宫颈癌患者中取得了 45.5% 的ORR 和 90.9% 的DCR,数据优异,且安全性可控。公司自主研发的StemTexp 扩增技术声称能更好地保持T细胞的干性。
其他管线:GT201,处于1期临床。属于第二代基因工程化TIL,表达膜结合IL-15。1期临床数据显示在多线治疗失败的实体瘤患者中ORR达到 55.6%,在头颈癌亚组中更是达到了100%的ORR(小样本量)。

3. 君赛生物 (Juncell Therapeutics)
上海君赛生物科技有限公司成立于2019年,致力于开发可覆盖多种类型晚期实体肿瘤的高品质、高可及性TIL细胞新药。
核心产品 GC101 是全球首款无需高强度清淋化疗、无需IL-2给药的TIL疗法,目前针对多种晚期实体瘤处于临床2期研究阶段,有望成为中国首个获批上市的TIL疗法。
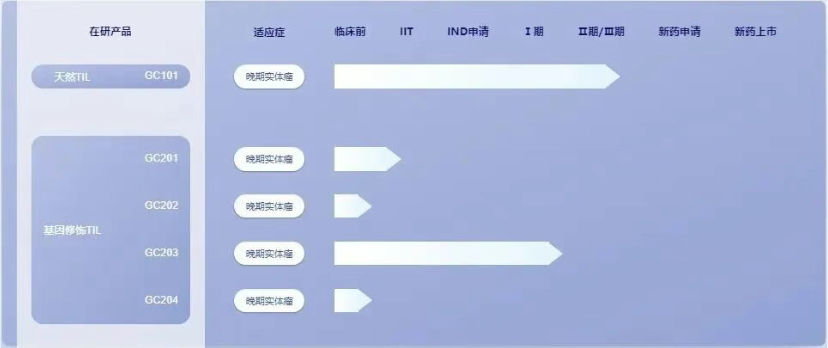
4. Obsidian Therapeutics
核心管线:OBX-115
技术特点:OBX-115 是一款基于“cytoDRiVE”平台开发的基因工程化TIL。其核心在于转入了一个膜结合的白介素-15(mbIL-15)基因,且该基因的表达受一种小分子药物(乙酰唑胺)的调控。这种设计旨在利用IL-15替代高毒性的IL-2,实现T细胞的自我维持与增殖。
临床阶段:正在进行1/2期临床试验(Agni-01)。
关键临床数据:疗效方面,在免疫检查点抑制剂耐药的晚期黑色素瘤患者中,OBX-115在RP2D(推荐2期剂量)下显示出 67% 的ORR,且包括完全缓解(CR)病例。这一数据在数值上显著优于第一代未修饰TIL。安全性方面,最具颠覆性的是其安全性数据。试验中未观察到与治疗相关的Grade 4非血液学毒性,无ICU转入需求。这意味着TIL疗法有望走出ICU,在普通病房甚至门诊进行,极大地降低了医疗资源消耗。
5. KSQ Therapeutics —— CRISPR基因编辑TIL
核心管线:KSQ-001EX
技术特点:利用CRISPR/Cas9技术敲除TIL细胞中的 SOCS1 基因。SOCS1(细胞因子信号转导抑制因子1)是T细胞内的一种“刹车”蛋白,敲除它相当于解除了T细胞的限制,使其对细胞因子更敏感,增殖能力更强,抗肿瘤活性更持久。
临床阶段:1/2期临床试验(NCT06237881)正在招募黑色素瘤、头颈癌和肺癌患者。
研发逻辑:KSQ利用其专有的CRISPRomics平台筛选出SOCS1作为最佳靶点。临床前数据显示,SOCS1敲除的TIL在实体瘤模型中的持久性和杀伤力远超野生型TIL。这代表了利用基因编辑技术改造TIL内在生物学特性的最前沿方向。
四、BD交易情况
TIL疗法领域的 BD 活动并不活跃,从2019年到目前为止统计到的TIL疗法相关交易为四起,均未提供交易金额,中国管线尚未报道相关交易。
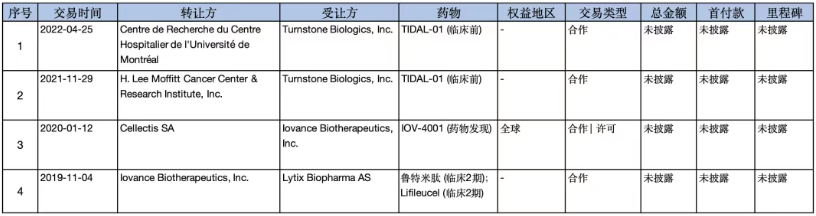
五、技术展望
基于对当前管线临床效果,特别是Iovance获批后的真实世界表现,及Obsidian、KSQ等二代产品的初步数据分析,TIL疗法的未来发展将呈现以下三大趋势:
5.1 从“野生型”向“工程化 2.0”的全面迭代
第一代TIL虽然有效,但其对高剂量IL-2的依赖导致了严重的副作用(毛细血管渗漏综合征),限制了其在身体状况较差患者中的应用。
趋势:未来的TIL必将是基因修饰的。
膜结合细胞因子(mbIL-15):如Obsidian的OBX-115和沙砾生物的GT201,通过自带“干粮”(IL-15),使得TIL在体内无需外源性IL-2即可存活。这不仅能消除IL-2毒性,还有望提升疗效,使TIL疗法成为一种无需ICU支持的常规治疗手段。
基因编辑去抑制(CRISPR KO):如KSQ敲除SOCS1,或敲除PD-1、CISH等抑制性基因。通过永久解除T细胞的“刹车”,使其在免疫抑制的肿瘤微环境中仍能保持高昂的战斗力。
5.2 制造工艺的极速化与标准化
超过22天的漫长的生产周期是患者脱落的主要原因。
趋势:缩短培养周期至极限。
Iovance正在开发第3代工艺(Gen 3),试图将生产时间压缩至16天。
原理:缩短体外培养时间不仅能更快给药,更能保留T细胞的“干性”。研究表明,培养时间越长,T细胞越容易分化为终末效应细胞,回输后存活时间短;而年轻态、干性强的T细胞在体内扩增潜力更大,疗效更好。
非病毒载体递送:利用电转技术递送CRISPR核糖核蛋白(RNP)或转座子系统,替代昂贵且制备周期长的慢病毒载体,将大幅降低生产成本(COGS)。
5.3 适应症的拓展与联合治疗
虽然黑色素瘤已获批,但对于市场更大的肺癌、消化道肿瘤,单纯TIL疗效仍有瓶颈。
趋势:联合治疗:TIL + PD-1抗体已成为标配。未来将探索TIL + 溶瘤病毒(如TILT Biotherapeutics的策略)、TIL + 表观遗传调控药物的联合,以改善肿瘤微环境,为TIL“开路”。
合成生物学介入:如RootPath公司提出的技术,不直接扩增TIL,而是测序TIL中的TCR,筛选出最高亲和力的TCR序列,再利用合成生物学方法转导至健康的新鲜T细胞中(类似于TCR-T,但靶点源自个体化TIL)。这种方式可能规避肿瘤来源T细胞本身质量差的问题,代表了TIL与TCR-T技术的终极融合。
References:
1. FDA grants accelerated approval to lifileucel for unresectable or metastatic melanoma.
2. First Cancer TIL Therapy Gets FDA Approval for Advanced Melanoma.
3. Obsidian Therapeutics Announces Positive Interim Top-Line Clinical Data for OBX-115 Engineered TIL Cell Therapy in Advanced or Metastatic Melanoma Post-Anti-PD1 Therapy.
4. Iovance Biotherapeutics官网。
5. 沙砾生物官网。
6. 君赛生物官网
7. Obsidian Therapeutics官网
8. KSQ Therapeutics官网.
9. Tumour-infiltrating lymphocyte therapy landscape: prospects and challenges - PMC.
10. The Latest On CRISPR Deployment In TIL Therapy Development - Cell and Gene.
...